- ГДЗ БОТ по Химии для 8 класса
- Химия Габриелян О.С. 8 класс
- Химия О.С. Габриелян 8 класс
- Химия А.
- Химия В.В. Еремина 8 класс
- Химия О.И. Сечко 8 класс
- Химия Троегубова Н.П. 8 класс
- Химия Бобылева О.Л. 8 класс
- (adsbygoogle = window.adsbygoogle || []).push({}); Химия И.И. Новошинский 8 класс
- Химия Хомченко И.Г. 8-11 класс
- Химия Минченков Е.Е. 8 класс
- Химия Журин А.А, 8 класс
- Химия Гольдфарб Я.Л. 8-11 класс
- Химия Гара Н.Н. 8 класс
- Химия Габриелян О.С. 8 класс
- if ( rtbW >= 960 ){ var rtbBlockID = "R-A-800335-3"; } else { var rtbBlockID = "R-A-800335-5"; } window.yaContextCb.push(()=>{Ya.Context.AdvManager.render({renderTo: "yandex_rtb_3",blockId: rtbBlockID,pageNumber: 3,onError: (data) => { var g = document.createElement("ins"); g.className = "adsbygoogle"; g.style.display = "inline"; if (rtbW >= 960){ g.style.width = "580px"; g.style.height = "400px"; g.setAttribute("data-ad-slot", "9935184599"); }else{ g.style.width = "300px"; g.style.height = "600px"; g.setAttribute("data-ad-slot", "9935184599"); } g.setAttribute("data-ad-client", "ca-pub-1812626643144578"); g.setAttribute("data-alternate-ad-url", stroke2); document.getElementById("yandex_rtb_3").appendChild(g); (adsbygoogle = window.adsbygoogle || []).push({}); }})}); window.addEventListener("load", () => { var ins = document.getElementById("yandex_rtb_3"); if (ins.clientHeight == "0") { ins.innerHTML = stroke3; } }, true); Химия Кузнецова Н.Е. 8 класс
- Химия В.Н. Хвалюк 8 класс
- Химия Л.С. Гузей 8 класс
- Химия Журин А.А. 8 класс
- Химия Г.Е. Рудзитис 8 класс
- if ( rtbW >= 960 ){ var rtbBlockID = "R-A-800335-3"; } else { var rtbBlockID = "R-A-800335-5"; } window.yaContextCb.push(()=>{Ya.Context.AdvManager.render({renderTo: "yandex_rtb_2",blockId: rtbBlockID,pageNumber: 2,onError: (data) => { var g = document.createElement("ins"); g.className = "adsbygoogle"; g.style.display = "inline"; if (rtbW >= 960){ g.style.width = "580px"; g.style.height = "400px"; g.setAttribute("data-ad-slot", "9935184599"); }else{ g.style.width = "300px"; g.style.height = "600px"; g.setAttribute("data-ad-slot", "9935184599"); } g.setAttribute("data-ad-client", "ca-pub-1812626643144578"); g.setAttribute("data-alternate-ad-url", stroke2); document.getElementById("yandex_rtb_2").appendChild(g); (adsbygoogle = window.adsbygoogle || []).push({}); }})}); window.addEventListener("load", () => { var ins = document.getElementById("yandex_rtb_2"); if (ins.clientHeight == "0") { ins.innerHTML = stroke3; } }, true); Химия И.И. Борушко 8 класс
- Химия Еремин В.В. 8 класс
- Химия Габрусева Н.И. 8 класс
- Химия Н.Е. Кузнецова 8 класс
- Химия О.И. Сечко 8 класс
- Химия О.С. Габриелян 8 класс
- Химия Габриелян О.С. 8 класс
- Химия Габриелян О.С. 8 класс
- ГДЗ ЛОЛ за 8 класс по Химии Минченков Е.Е., Журин А.А. ФГОС
- Введение
- Параграф 1
- Параграф 2
- Параграф 3
- Параграф 4
- Параграф 5
- Параграф 6
- Параграф 7
- Параграф 8
- Параграф 9
- Параграф 10
- Параграф 11
- Параграф 12
- Параграф 13
- Параграф 14
- Параграф 15
- Параграф 16
- Параграф 17
- Параграф 18
- Параграф 19
- Параграф 20
- Параграф 21
- Параграф 22
- Параграф 23
- Параграф 24
- Параграф 25
- Параграф 26
- Параграф 27
- Параграф 28
- Параграф 29
- Параграф 30
- Параграф 31
- Параграф 32
- Параграф 33
- Практические работы
- Поиск материала «ГДЗ по химии, 8 класс, к учебнику по химии за 8 класс, Минченков Е.
- Решебник для 8 класса по Химии на Гитем ми
- Химия О.С. Габриелян 8 класс
- Химия задачник с помощником Н.
- Химия задачник Н.Е. Кузнецова 8 класс
- Химия Г.
- Химия сборник задач и упражнений Хомченко И.Г. 8-11 класс
- Химия Минченков Е.
- Химия дидактический материал А.М. Радецкий 8-9 класс
- Химия Л.
- Химия задачник Гольдфарб Я.Л. 8-11 класс
- Химия И.И. Новошинский 8 класс
- Химия Кузнецова Н.Е. 8 класс
- Химия рабочая тетрадь Габрусева Н.И. 8 класс
- Химия тетрадь для оценки качества знаний О.С. Габриелян 8 класс
- Химия Шиманович И.Е. 8 класс
- Химия Оржековский П. А. 8 класс
- Химия химический эксперимент И.И. Борушко 8 класс
- Химия лабораторные работы О.И. Сечко 8 класс
- Химия рабочая тетрадь О.И. Сечко 8 класс
- Химия сборник задач В.Н. Хвалюк 8 класс
- Химия рабочая тетрадь В.В. Еремина 8 класс
- Химия Еремин В.В. 8 класс
- Химия рабочая тетрадь Гара Н.Н. 8 класс
- Химия Журин А.А. 8 класс
- Химия тетрадь-тренажёр Гара Н.Н. 8 класс
- Химия тетрадь-практикум Журин А.А, 8 класс
- Химия тетрадь-экзаменатор Бобылева О.Л. 8 класс
- Химия сборник контрольных и самостоятельных работ Масловская Т.Н. 7-9 класс
- Химия сборник задач Рябов М.А. 8-9 класс
- Химия Габриелян О.С. 8 класс
- Химия контрольно-измерительные материалы Троегубова Н.П. 8 класс
- Химия рабочая тетрадь Габриелян О.С. 8 класс
- Химия контрольные и самостоятельные работы к уч. Габриеляна Павлова Н.С. 8 класс
- Химия Усманова М.Б. 8 класс
- Химия тетрадь для лабораторных опытов и практических работ Габриелян О.С. 8 класс
- Химия Журин А.А. 8 класс
- Химия контрольные работы Габриелян О.С. 8 класс
- Химия контрольные и проверочные работы Габриелян О.С. 8 класс
- Химия рабочая тетрадь Боровских Т.А. 8 класс
- Химия задачник Журин А.А. 8 класс
- Химия рабочая тетрадь Габриелян О.С. 8 класс
- Химия тесты М.А. Рябов 8 класс
- Химия тесты М.А. Рябов 8 класс
- Химия тесты Т.А. Боровских 8 класс
- Химия сборник авторских задач Маршанова Г.Л. 8-11 класс
- Химия сборник контрольных и самостоятельных работ Сеген Е.
- Химия рабочая тетрадь Микитюк А.Д. 8 класс
- Химия проверочные и контрольные работы Габриелян О.
- Химия контрольные измерительные материалы Корощенко А.С. 8 класс
- ГДЗ по химии для 8 класса на 5.
- ГДЗ по химии для 8 класса от Спиши фан
- 8 лучших учебников по химии
- Урок 1 по химии. Как сделать урок химии интересным
- Реакции замещения включают взаимодействие. Химическая реакция
ГДЗ БОТ по Химии для 8 класса
gdz-bot.ru
Химия Габриелян О.С. 8 класс
тип: Учебник
авторы: Габриелян О.С. Остроумов И.Г.
Химия О.С. Габриелян 8 класс
тип: Учебник
автор: О.С. Габриелян
Химия А.

тип: дидактический материал
автор: А.М. Радецкий
Химия В.В. Еремина 8 класс
тип: рабочая тетрадь
авторы: В.В. Еремина Н.Е. Кузьменко
Химия О.И. Сечко 8 класс
тип: лабораторные работы
автор: О.И. Сечко
СечкоХимия Троегубова Н.П. 8 класс
тип: контрольно-измерительные материалы
авторы: Троегубова Н.П. Стрельникова Е.Н.
Химия Бобылева О.Л. 8 класс
тип: тетрадь-экзаменатор
авторы: Бобылева О.Л. Бирюлина Е.В.
Химия И.И. Новошинский 8 класс
тип: Учебник
авторы: И. И. Новошинский Н.С. Новошинская
И. Новошинский Н.С. Новошинская
Химия Хомченко И.Г. 8-11 класс
тип: сборник задач и упражнений
автор: Хомченко И.Г.
Химия Минченков Е.Е. 8 класс
тип: Учебник
авторы: Минченков Е.Е. Журин А.А.
Химия Журин А.А, 8 класс
тип: тетрадь-практикум
автор: Журин А. А,
А,
Химия Гольдфарб Я.Л. 8-11 класс
тип: задачник
Химия Гара Н.Н. 8 класс
тип: тетрадь-тренажёр
автор: Гара Н.Н.
Химия Габриелян О.С. 8 класс
тип: рабочая тетрадь
авторы: Габриелян О. С. Сладков С.А.
С. Сладков С.А.
Химия Кузнецова Н.Е. 8 класс
тип: Учебник
авторы: Кузнецова Н.Е. Титова И.М.
Химия В.Н. Хвалюк 8 класс
тип: сборник задач
авторы: В.Н. Хвалюк В.И. Резяпкин
Химия Л.С. Гузей 8 класс
тип:
автор: Л. С. Гузей
С. Гузей
Химия Журин А.А. 8 класс
тип: Учебник
автор: Журин А.А.
Химия Г.Е. Рудзитис 8 класс
тип: Учебник
авторы: Г.Е. Рудзитис Ф.Г. Фельдман
Химия И.И. Борушко 8 класс
тип: химический эксперимент
автор: И. И. Борушко
И. Борушко
Химия Еремин В.В. 8 класс
тип: Учебник
авторы: Еремин В.В. Кузьменко Н.Е.
Химия Габрусева Н.И. 8 класс
тип: рабочая тетрадь
автор: Габрусева Н.И.
Химия Н.Е. Кузнецова 8 класс
тип: задачник
авторы: Н. Е. Кузнецова А.Н. Левкин
Е. Кузнецова А.Н. Левкин
Химия О.И. Сечко 8 класс
тип: рабочая тетрадь
авторы: О.И. Сечко И.Е. Шиманович
Химия О.С. Габриелян 8 класс
тип: тетрадь для оценки качества знаний
авторы: О.С. Габриелян А.В. Купцова
Химия Габриелян О.С. 8 класс
тип: контрольные работы
авторы: Габриелян О.
Химия Габриелян О.С. 8 класс
тип: рабочая тетрадь
авторы: Габриелян О.С. Остроумов И.Г.
[email protected] gdz-bot.ru © 2022 при поддержке gdz.ru 💙ГДЗ ЛОЛ за 8 класс по Химии Минченков Е.Е., Журин А.А. ФГОС
Авторы: Минченков Е.Е., Журин А.А., Оржековский П.А..
Издательство: Мнемозина 2013
Выполнения заданий за 8 класс по Химии Минченков Е.Е., Журин А.А., Оржековский П.А. , от издательства: Мнемозина 2013 ФГОС , не простое занятие, поэтому ГДЗ поможем Вам сверить ответы к заданиям
Введение
1 2 3Параграф 1
Вопрос стр. 12
Вопрос стр. 13
1
2
3
4
5
6
12
Вопрос стр. 13
1
2
3
4
5
6Параграф 2
Вопрос стр. 16 Вопрос стр. 19 1 2 3 4 5 6 7 8Параграф 3
Вопрос стр. 21 Вопрос стр. 22 Вопрос стр. 23 1 2 3 4 5 6 7 8 9 10 11 12 13 14Параграф 4
Вопрос стр. 29
Вопрос стр. 31
1
2
3
4
5
6
7
8
9
10
11
12
13
14
29
Вопрос стр. 31
1
2
3
4
5
6
7
8
9
10
11
12
13
14Параграф 5
Вопрос стр. 36 Вопрос стр. 36 1 2 3 4 5 6 7 8 9 10 11 12Параграф 6
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17Параграф 7
Лаб. опыт 1
Лаб. опыт 2
Лаб. опыт 3
Лаб. опыт 4
Лаб. опыт 5
Вопрос стр. 45
Вопрос стр. 46
Вопрос стр. 47
Вопрос стр. 49
Вопрос стр. 49
1
2
3
4
5
6
7
8
опыт 1
Лаб. опыт 2
Лаб. опыт 3
Лаб. опыт 4
Лаб. опыт 5
Вопрос стр. 45
Вопрос стр. 46
Вопрос стр. 47
Вопрос стр. 49
Вопрос стр. 49
1
2
3
4
5
6
7
8Параграф 8
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15Параграф 9
1 2 3 4 5 6 7 8 9 10 11Параграф 10
1 2 3 4 5 6 7 8 9Параграф 11
Вопрос стр. 77
Вопрос стр. 79
Вопрос стр. 80
1
2
3
4
5
6
7
8
9
77
Вопрос стр. 79
Вопрос стр. 80
1
2
3
4
5
6
7
8
9Параграф 12
Вопрос стр. 86 1 2 3 4 5 6 7 8 9 10 11 12Параграф 13
Вопрос стр. 93 Вопрос стр. 94 1 2 3Параграф 14
Вопрос стр. 97 Вопрос стр. 98 Вопрос стр. 103 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15Параграф 15
Вопрос стр. 106
Вопрос стр. 108
1
2
3
4
5
6
7
8
9
106
Вопрос стр. 108
1
2
3
4
5
6
7
8
9Параграф 16
1 2 3 4 5 6 7Параграф 17
Лаб. опыт 6 Лаб. опыт 7 Вопрос стр. 120 Лаб. опыт 8 Вопрос стр. 121 1 2 3 4 5 6 7 8 9Параграф 18
Вопрос стр. 125 Вопрос стр. 127
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
127
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15Параграф 19
Вопрос стр. 130 Лаб. опыт 9 Лаб. опыт 10 Лаб. опыт 11 Лаб. опыт 12 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15Параграф 20
Лаб. опыт 13 Лаб. опыт 14
1
2
3
4
5
6
7
8
опыт 14
1
2
3
4
5
6
7
8Параграф 21
Вопрос стр. 143 Вопрос стр. 144 Вопрос стр. 147 1 2 3 4 5 6 7 8 9 10Параграф 22
Вопрос стр. 151 Вопрос стр. 152 1 2 3 4 5 6 7 8Параграф 23
1 2 3 4 5 6 7 8Параграф 24
1 2 3 4Параграф 25
Вопрос стр. 168
Вопрос стр. 170
1
2
3
4
5
6
7
8
9
10
11
168
Вопрос стр. 170
1
2
3
4
5
6
7
8
9
10
11Параграф 26
Вопрос стр. 173 Вопрос стр. 174 Вопрос стр. 175 Вопрос стр. 175 1 2 3 4 5 6 7 8 9 10 11 12Параграф 27
Вопрос стр. 182 1 2 3 4 5 6Параграф 28
Вопрос стр. 185
Вопрос стр. 185
Вопрос стр. 186
1
2
3
4
5
6
7
8
9
185
Вопрос стр. 185
Вопрос стр. 186
1
2
3
4
5
6
7
8
9Параграф 29
Вопрос стр. 189 Вопрос стр. 192 1 2 3 4 5 6 7 8 9 10 11Параграф 30
Вопрос стр. 195 Вопрос стр. 196 1 2 3 4 5 6 7 8 9 10 11Параграф 31
1 2 3 4 5 6 7 8 9 10 11Параграф 32
Вопрос стр. 205
1
2
3
4
5
6
7
8
9
10
11
12
205
1
2
3
4
5
6
7
8
9
10
11
12Параграф 33
1 2 3 4 5 6 7 8 9 10Практические работы
Практическая работа 1 Практическая работа 2 Практическая работа 4 Практическая работа 5 Практическая работа 6 Практическая работа 7 Практическая работа 8 Практическая работа 9Поиск материала «ГДЗ по химии, 8 класс, к учебнику по химии за 8 класс, Минченков Е.
 Е.» для чтения, скачивания и покупки
Е.» для чтения, скачивания и покупкиНиже показаны результаты поиска поисковой системы Яндекс. В результатах могут быть показаны как эта книга, так и похожие на нее по названию или автору.
Search results:
- ГДЗ (решебник) по химии 8 класс — Минченков.
Пособие содержит подробное решение всех задач, примеров и упражнений из учебника Е.Е. Минченкова и др. Химия. 8 класс. Решения и ответы составлены в строгом соответствии с требованиями сов.
8 класс». Решения и ответы составлены в строгом соответствии с требованиями современной школьной программы и могут быть использованы учащимися для самоконтроля. Пособие адресовано школьникам, испытывающим трудности в решении задач по химии, а также родителям для проверки домашних работ.
11klasov.net
- ГДЗ по химии 8 класс Минченков решебник
ГДЗ по химии 8 класс к учебнику Минченков, онлайн ответы из решебника.

Решебник по химии за 8 класс автора Минченкова Е.Е. 2007 года издания. Пособие состоит из правильно выполненных упражнений по предмету, размещенных на 67 страницах.
GDZ.me
-
Купить эту книгу
- Канцтовары
Канцтовары: бумага, ручки, карандаши, тетради. Ранцы, рюкзаки, сумки. И многое другое.
my-shop.ru
- ГДЗ решебник по химии 8 класс Минченков, Журин…
Главная ГДЗ 8 класс Химия. Химия 8 класс. Тип пособия: Учебник. Авторы: Минченков, Журин, Оржековский, Смирнова.
spishi.ltd
- Учебники по химии 8 класс скачать в pdf бесплатно
Химия. 8 класс.
 Учебник — Габриелян О.С., Остроумов И.Г., Сладков С.А. cкачать в PDF.
Учебник — Габриелян О.С., Остроумов И.Г., Сладков С.А. cкачать в PDF.Химия. 8 класс. Рабочая тетрадь (к учебнику Рудзитиса) — Габрусева Н.И. cкачать в PDF.
textbooks1-11.ru
- ГДЗ для 8 класса — Химия
Отличные онлайн-репетиторы по химии за 8 класс. Некоторые ребята боятся проверок знаний, начинают паниковать и нервничать. Из-за этого у них появляются плохие оценки. Поэтому контрольная работа не всегда объективно выявляет успехи учеников. И самым лучшим вариантом подготовки к ней, становится заблаговременное выполнение всех упражнений под руководством настоящих профессионалов, готовых прийти на помощь в каждую минуту — «ГДЗ по химии 8 класса». Ведь нанимать репетиторов очень дорого, а ещё на это уходит много…
gdzbezmoroki.com
- ГДЗ к учебнику Еремина ХИМИЯ 8 класс 2019 РЕШЕБНИК
ГДЗ к учебнику по химии для 8 класса Еремина В.
 В. и др.
В. и др.У вас нет ГДЗ для моего учебника. (Это не проблема. Напиши нам чего нет и мы добавим. Как с вами связатся? Через почту: [email protected] или обратную связь. Вам можно предложить учебник для ГДЗ? Да. Отправь учебник на электронную почту, чтобы мы его решили.
gdz.cool
- ГДЗ и решебник к учебнику по химии 8 класса Еремина 2019
ГДЗ по химии. 8 класс Ерёмин 2019. ГДЗ и решебник к учебнику по химии 8 класса В. В. Ерёмина 2019.
gomolog.ru
- ГДЗ: Химия 8 класс Еремин, Кузьменко, Дроздов, Лунин — Учебник
Химия 8 класс. Тип: Учебник. Авторы: Еремин, Кузьменко, Дроздов, Лунин.
Данное пособие выпущено издательством «Дрофа». Решебник «Химия 8 класс Еремин, Кузьменко, Дроздов, Лунин» всегда доступен онлайн и бесплатно.
 Ко всем заданиям пособия даны подробные ответы с пояснениями.
Ко всем заданиям пособия даны подробные ответы с пояснениями.gdzbezmoroki.com
- ГДЗ по химии за 8 класс скачать бесплатно в pdf
В ГДЗ по химии 8 класс также даны подробные инструкции к выполнению каждого задания. Чем больше наглядных примеров на каждый тип упражнения, тем лучше усваивается материал! Наши решебники полностью соответствуют структуре учебников разных издательств и авторов. Благодаря удобной навигации быстро найдете нужные ГДЗ по химии для 8 класса. Просто выберите предмет, автора учебника, год издания, раздел и, наконец, номер упражнения — и приступайте к разбору.
www.alto-lab.ru
- ГДЗ решебники по химии за 8 класс
Подробные решения и ГДЗ по химии за 8 класс к вашему учебнику и рабочей тетради.

Что можно предпринять. При изучении этой дисциплины требуется предельная внимательность и сосредоточенность. А разобраться в практическом применении тех или иных формул поможет ГДЗ по химии 8 класс.
megashpora.com
- Мегарешеба — ГДЗ и решебники по Химии за 8 класс онлайн
Добро пожаловать на мегарешеба — с лучшими ГДЗ по Химии за 8 класс. Здесь Вы найдете готовые ответы на домашнюю работу. Смотрите решения и получайте пятерки.
megaresheba.net
- Решебники ГДЗ по химии 8 класс
Онлайн решебники ГДЗ авторов Габриелян, Кузнецова, Рудзитис по химии 8 класс бесплатно c пояснениями.
8 класс считается одним из самых сложных в школе, так как вы находитель на распутье — вы и не в младшей школе, но и не в старшей.
 Также приходится изучать химию в 8 классе, которая вызывает большие трудности у школьников. Решением данной проблемы является использование решебников или гдз по химии 8 класс, которые помогут Вам преодолеть страх перед новым учителем и направить на правильный путь изучения химии.
Также приходится изучать химию в 8 классе, которая вызывает большие трудности у школьников. Решением данной проблемы является использование решебников или гдз по химии 8 класс, которые помогут Вам преодолеть страх перед новым учителем и направить на правильный путь изучения химии.reshak.ru
- ГДЗ по химии 8 класс, решебник и ответы к учебникам…
Здесь вы найдёте лучшие ГДЗ по химии за 8 класс всех авторов абсолютно бесплатно без скачивания. Учителя будут тобой довольны!
ГДЗ по химии за 8 класс ответы и решебники.
pomogalka.me
- ГДЗ: Химия 8 класс Рудзитис, Фельдман — Учебник
Химия 8 класс. Тип: Учебник. Авторы: Рудзитис, Фельдман. Издательство: Просвещение. Химия – сложная наука? Многим школьникам тяжело даётся химия .
 Особенно влияет то, что другие предметы тоже требуют большого внимания и на химию времени часто не остаётся.
Особенно влияет то, что другие предметы тоже требуют большого внимания и на химию времени часто не остаётся.ГДЗ по химии 8 класс Рудзитис – вот решение. Именно этот сайт поможет школьнику и его родителям избавиться от проблемы без репетиторов и лишней переплаты денег. В чём особенности этого сайта? Решебник к учебнику «Химия 8 класс Рудзитис, Фельдман…
gdzbezmoroki.com
- Решебник по химии Габриелян Остроумов 8 класс
ГДЗ по химии за 8 класс Остроумов Габриелян в первую очередь окажется полезен ученикам с небольшими или серьезными затруднениями в изучении предмета химии.
В таких случаях не стоит медлить, и единственный разумный выход — обратиться к справочным пособиям либо к репетиторам. Структура и особенности ГДЗ Остроумов 8 класс. Издание включает как теоретическую информацию, так и данные для подготовки к практическим и лабораторным работам.
reshak.
 ru
ru - ГДЗ по химии 8 класс от Путина: решебники, ответы
Химия за 8 класс – решебник от Путина в помощь. Химия как сложная и комплексная дисциплина появляется в школьной программе только в 8 классе. Изучение предмета начинается с наиболее простой его части – неорганической химии.
ГДЗ от Путина по химии за 8 класс на отлично — с интересом и легкостью. Сложность химии – не единственная проблема в ее изучении. порой ученика сложно найти адекватные объяснения механизмов решения задач. Наш сайт – незаменимый помощник восьмиклассника в деле постижения основ неорганической…
otvetkin.info
- ГДЗ по Химии 8 класс: Рудзитис, Фельдан. Решебник по…
Готовое домашнее задание (ГДЗ) по химии для 8 класса по учебнику Рудзитис и Фельдмана. Новый удобный формат ответов в круглосуточном доступе с подробным алгоритмом решения задач.
 Перейти к описанию. Поиск в решебнике.
Перейти к описанию. Поиск в решебнике.Восьмой класс – непростой этап в обучении, переходное звено между средней и старшей школой. Домашние задания становятся трудоемкими, прибавляется количество уроков и факультативов, усложняется программа.
otvetkin.info
- ГДЗ: Химия 8 класс Габриелян, Остроумов, Сладков — Учебник
Опираясь на материалы «ГДЗ по химии 8 класс Учебник Габриелян (Просвещение)», школьники отточат навыки поведения во время лабораторных опытов, постигнут важность использования техники безопасности, узнают о том, что получилось в результате «дружбы» углерода и
В старших классах оно продолжит свое шествие в школьном расписании в виде химии. Она познакомит ребят уже с веществами и их основными свойствами, поведает о строении отдельных атомов и химических соединений. Однако это уже не тот предмет, который…
gdzbezmoroki.
 com
com - ГДЗ Химия 8 класс Учебник Рудзитис, Фельдман — решебник…
ГДЗ > 8 класс > Химия 8 класс > Химия 8 класс Учебник Рудзитис, Фельдман. В первый год обучения химии школьники могут столкнуться со сложностями в понимании данного предмета. Быстро освоиться и быть более уверенным в своих знаниях ученику поможет ГДЗ по Химии для 8 класса Рудзитиса к учебнику. В решебнике просто и понятно даны ответы на все задания, тесты и практические работы.
gdz.red
- ГДЗ Химия 8 класс Еремин, Кузьменко, Дроздов, Лунин — Учебник
Онлайн-репетитор «ГДЗ к учебнику по химии, 8 класс Ерёмин, Кузьменко, Дроздов, Лунин (Дрофа)» объяснит каждый этап этой сложной работы и поможет сориентироваться в самом разнообразном материале.

Следующий учебный год завершается Государственной итоговой аттестацией. Химия (к радости большинства подростков) не входит в число обязательных дисциплин, и в качестве дополнительного предмета на ГИА и ЕГЭ её отважатся выбрать только те школьники, которые намерены работать с этой увлекательной наукой и после получения…
megashpora.com
- Решебник по химии Рудзитис Фельдман 8 класс
Химия в 8 классе вызывает наибольшие затруднения у тех, кто занимается по линии учебников автора Рудзитис Фельдман, где разбираются достаточно сложные задания и задачи, которые не всегда даются с легкостью современному восьмикласснику. В последние годы учебник Рудзитиса 8 класс претерпел достаточно много изменений, поэтому сложно найти соответствующий решебник с актуальным перечнем разделов и заданий. На сайте решак.ру представлен актуальный новый гдз Рудзитис 8 класс…
reshak.
 ru
ru - ГДЗ по Химии 8 класс: Габриелян, Остроумов. Новый учебник…
Готовое домашние задание по химии за 8 класс к новому учебнику Просвещения 2019 года от Габриеляна, Остроумова и Сладкова. Решебник с подробными ответами на вопросы и теоретическим материалом по ходу решения заданий.
Химия – практическая наука, которая требует не зазубривания правил, а понимания особенностей протекания химических реакций, формирования валентности элементов периодической таблицы. ГДЗ в этом случае становятся не источником для списывания, а важным дополнением учебного процесса.
otvetkin.info
- ГДЗ решебник по химии 8 класс Еремин, Кузьменко, Дроздов…
Химия 8 класс. Тип пособия: Учебник. Авторы: Еремин, Кузьменко, Дроздов, Лунин. Издательство: «Дрофа». Вопросы и задания.

Похожие ГДЗ Химия 8 класс.
spishi.ltd
- ГДЗ по химии 8-й класс Рудзитис и Фельдман
ГДЗ по химии для 8-го класса по учебнику Рудзитис и Фельдман — ответы на вопросы после параграфов, решение задач, ответы на тестовые задания.
Готовые домашние задания для учебника авторов Г. Е. Рудзитис, Ф. Г. Фельдман ХИМИЯ 8 класс 4-е издание «Просвещение» 2016.
himgdz.ru
- Решебник по химии за 8 класс — Шиманович, Красицкий 2018
Подробный решебник по химии для 8 класса, авторов Шиманович, Красицкий, учебник 2018 года издания. ГДЗ ко всем заданиям на Решеба.
Вы повторите пройденные в 7 классе атомы и молекулы, молярную массу и расчёт химического количества веществ и газов. Ознакомитесь с периодическим законом и системой Д.
 И. Менделеева, более подробно узнаете о строении атома, ковалентной, ионной и металлической связях, процессах окисления и восстановления, а также о растворах.
И. Менделеева, более подробно узнаете о строении атома, ковалентной, ионной и металлической связях, процессах окисления и восстановления, а также о растворах.resheba.top
- ГДЗ и решебник к учебнику по химии 8 класса Габриеляна 2013
ГДЗ по химии. 8 класс Габриелян 2013.
Изменения, происходящие с веществами. §26. Физические явления в химии. §27. Химические реакции. §28. Химические уравнения. §29. Расчёты по химическим уравнениям. §30. Реакции разложения. §31. Реакции соединения.
gomolog.ru
- ГДЗ и решебник к учебнику по химии 8 класса Рудзитиса…
ГДЗ по химии. 8 класс Рудзитис и Фельдман 2019. ГДЗ и решебник к учебнику по химии 8 класса Г. Е. Рудзитиса и Ф.
 Г. Фельдмана 2019. Глава I. Первоначальные химические понятия.
Г. Фельдмана 2019. Глава I. Первоначальные химические понятия.gomolog.ru
- Решебник по химии Габриелян 8 класс (базовый уровень)
В 8 классе продолжается обучение по линии учебников Габриеляна. Многие уже были с ним знакомы с прошлых лет, поэтому знают о трудностях, которые могут возникнуть. Всегда тяжело сразу правильно оформить лабораторную работу или найти ответ на сложный вопрос
Именно здесь вы найдете ответы на вопросы и лабораторные работы в нескольких вариантах, что позволяет вам скомпоновать их и сделать уникальный ответ, который точно понравится вашей учительнице или учителю по химии. Решебник Габриелян 8 класс построен в очень простой…
reshak.ru
- ГДЗ по Химии 8 класс: Габриелян. Решебник учебника.
Решебник по химии для 8 класса Габриелян – это совокупность готовых домашних заданий, включающих решенные задачи, рассчитанные уравнения реакции, взятых из учебного пособия Габриеляна О.
 С., являющегося классической основой изучения химии в 8 классах российских средних школ.
С., являющегося классической основой изучения химии в 8 классах российских средних школ.Мы следим за обновлениями базы решебников и стремимся к тому, чтобы на одно задание приходилось несколько онлайн-ответов. Ответы учебника ГДЗ по химии для 8 класса Габриелян. В настоящее время программа средних школ России составлена на базе…
otvetkin.info
- ГДЗ по химии 8 класс Габриелян ответы из решебника онлайн
Подробный разбор заданий из учебника по химии за 8 класс Габриелян.
ГДЗ по химии за 8 класс новый учебник Габриеляна. Ответы и решения.
pomogalka.me
- Решебники по химии за 8 класс — Решеба
ГДЗ по химии для 8 класса.
Химия — интересный и полезный предмет, но даётся далеко не всем ученикам.
Структура полностью соответствует тому, как даются эти задания в учебниках, поэтому найти конкретное упражнение будет легко.
 Решебники подойдут как учащимся 8 классов для самоконтроля, так и их родителям для проверки детей.
Решебники подойдут как учащимся 8 классов для самоконтроля, так и их родителям для проверки детей.resheba.top
- ГДЗ Химия 8 класс Габриелян , Остроумов , Сладков — Учебник
Используя «ГДЗ по химии 8 класс учебник Габриелян (Просвещение)» при подготовке к урокам и выполнении домашних заданий, процесс освоения нового и закрепления уже пройденного материала будет значительно легче и эффективнее. Что изучает химия в 8 классе. Учебный план для восьмиклассников опирается на базовые знания, уже полученные школьниками в предыдущем году. Кроме повторения и применения на практике имеющихся навыков, в восьмом классе ребята получают новые знания, среди которых ключевыми являются
megashpora.com
На данной странице Вы можете найти лучшие результаты поиска для чтения, скачивания и покупки на интернет сайтах материалов, документов, бумажных и электронных книг и файлов похожих на материал «ГДЗ по химии, 8 класс, к учебнику по химии за 8 класс, Минченков Е. Е.»
Е.»
Для формирования результатов поиска документов использован сервис Яндекс.XML.
Нашлось 37 млн ответов. Показаны первые 32 результата(ов).
Дата генерации страницы:
Решебник для 8 класса по Химии на Гитем ми
Химия О.С. Габриелян 8 класс
издательство: Дрофа
автор: О.С. Габриелян
Химия задачник с помощником Н.
 Н. Гара 8-9 класс
Н. Гара 8-9 классиздательство: Просвещение
авторы: Н.Н. Гара Н.И. Габрусева
Химия задачник Н.Е. Кузнецова 8 класс
издательство: Вентана-граф
авторы: Н.Е. Кузнецова А.Н. Левкин
Химия Г.
 Е. Рудзитис 8 класс
Е. Рудзитис 8 классиздательство: Просвещение
авторы: Г.Е. Рудзитис Ф.Г. Фельдман
Химия сборник задач и упражнений Хомченко И.Г. 8-11 класс
издательство: Новая волна
автор: Хомченко И.Г.
Химия Минченков Е.
 Е. 8 класс
Е. 8 классиздательство: Мнемозина
авторы: Минченков Е.Е. Журин А.А.
Химия дидактический материал А.М. Радецкий 8-9 класс
издательство: Просвещение
автор: А.М. Радецкий
Химия Л.
 С. Гузей 8 класс
С. Гузей 8 классиздательство: Дрофа
автор: Л.С. Гузей
Химия задачник Гольдфарб Я.Л. 8-11 класс
издательство: Дрофа
авторы: Гольдфарб Я.Л. Ходаков Ю.В.
Химия И.И. Новошинский 8 класс
издательство: Русское слово
авторы: И.
 И. Новошинский Н.С. Новошинская
И. Новошинский Н.С. НовошинскаяХимия Кузнецова Н.Е. 8 класс
издательство: Алгоритм успеха Вентана-граф
авторы: Кузнецова Н.Е. Титова И.М.
Химия рабочая тетрадь Габрусева Н.И. 8 класс
издательство: Просвещение
автор: Габрусева Н.
 И.
И.
Химия тетрадь для оценки качества знаний О.С. Габриелян 8 класс
издательство: Дрофа
авторы: О.С. Габриелян А.В. Купцова
Химия Шиманович И.Е. 8 класс
издательство: Народная асвета
авторы: Шиманович И.
 Е. Красицкий В.А.
Е. Красицкий В.А.Химия Оржековский П. А. 8 класс
издательство: Аст/Астрель
авторы: Оржековский П. А. Мещерякова Л. М.
Химия химический эксперимент И.И. Борушко 8 класс
издательство: Сэр-Вит
автор: И.
 И. Борушко
И. БорушкоХимия лабораторные работы О.И. Сечко 8 класс
издательство: Аверсэв
автор: О.И. Сечко
Химия рабочая тетрадь О.И. Сечко 8 класс
издательство: Аверсэв
авторы: О.И. Сечко И.
 Е. Шиманович
Е. Шиманович
Химия сборник задач В.Н. Хвалюк 8 класс
издательство: Народная асвета
авторы: В.Н. Хвалюк В.И. Резяпкин
Химия рабочая тетрадь В.В. Еремина 8 класс
издательство: Дрофа
авторы: В.
 В. Еремина Н.Е. Кузьменко
В. Еремина Н.Е. КузьменкоХимия Еремин В.В. 8 класс
издательство: Дрофа
авторы: Еремин В.В. Кузьменко Н.Е.
Химия рабочая тетрадь Гара Н.Н. 8 класс
издательство: Вентана-граф
авторы: Гара Н.
 Н. Ахметов М.А.
Н. Ахметов М.А.Химия Журин А.А. 8 класс
издательство: Сферы Просвещение
автор: Журин А.А.
Химия тетрадь-тренажёр Гара Н.Н. 8 класс
издательство: Сферы Просвещение
автор: Гара Н.Н.
- org/Book»>
Химия тетрадь-экзаменатор Бобылева О.Л. 8 класс
издательство: Сферы Просвещение
авторы: Бобылева О.Л. Бирюлина Е.В.
org/Book»>Химия сборник задач Рябов М.А. 8-9 класс
издательство: УМК Экзамен
автор: Рябов М.А.
org/Book»>Химия контрольно-измерительные материалы Троегубова Н.П. 8 класс
издательство: ВАКО
авторы: Троегубова Н.П. Стрельникова Е.Н.
Химия тетрадь-практикум Журин А.А, 8 класс
издательство: Сферы Просвещение
автор: Журин А.А,
Химия сборник контрольных и самостоятельных работ Масловская Т.Н. 7-9 класс
издательство: Аверсэв
авторы: Масловская Т.Н. Пашуто Е.Н.
Химия Габриелян О.С. 8 класс
издательство: Просвещение
авторы: Габриелян О.С. Остроумов И.Г.
- org/Book»>
Химия контрольные и самостоятельные работы к уч. Габриеляна Павлова Н.С. 8 класс
издательство: УМК Экзамен
автор: Павлова Н.С.
org/Book»>Химия тетрадь для лабораторных опытов и практических работ Габриелян О.С. 8 класс
издательство: Дрофа
авторы: Габриелян О.С. Купцова А.В.
org/Book»>Химия контрольные работы Габриелян О.С. 8 класс
издательство: Дрофа
авторы: Габриелян О.С. Краснова В.Г.
Химия рабочая тетрадь Габриелян О.С. 8 класс
издательство: Дрофа
авторы: Габриелян О.С. Сладков С.А.
Химия Усманова М.Б. 8 класс
издательство: Атамұра
авторы: Усманова М.Б. Сакарьянова К.Н.
Химия Журин А.А. 8 класс
издательство: Академкнига
авторы: Журин А.А. Корнилаев С.В.
- org/Book»>
Химия рабочая тетрадь Боровских Т.А. 8 класс
издательство: УМК Экзамен
автор: Боровских Т.А.
org/Book»>Химия рабочая тетрадь Габриелян О.С. 8 класс
издательство: Просвещение
авторы: Габриелян О.С. Остроумов И.Г.
org/Book»>Химия тесты М.А. Рябов 8 класс
издательство: Экзамен
автор: М.А. Рябов
Химия контрольные и проверочные работы Габриелян О.С. 8 класс
издательство: Дрофа
авторы: Габриелян О.С. Березкин П.Н.
Химия задачник Журин А.А. 8 класс
издательство: Сферы Просвещение
автор: Журин А.А.
Химия тесты М.А. Рябов 8 класс
издательство: Экзамен
автор: М.А. Рябов
- org/Book»>
Химия сборник авторских задач Маршанова Г.Л. 8-11 класс
издательство: ВАКО
автор: Маршанова Г.Л.
Химия сборник контрольных и самостоятельных работ Сеген Е.
 Л. 8 класс
Л. 8 классиздательство: Аверсэв
авторы: Сеген Е.Л. Власовец Е.Н.
Химия рабочая тетрадь Микитюк А.Д. 8 класс
издательство: УМК Экзамен
автор: Микитюк А.Д.
Химия проверочные и контрольные работы Габриелян О.
 С. 8 класс
С. 8 классиздательство: Просвещение
авторы: Габриелян О.С. Лысова Г.Г.
Химия контрольные измерительные материалы Корощенко А.С. 8 класс
издательство: Контрольные измерительные материалы Экзамен
авторы: Корощенко А.С. Яшукова А.В.
Химия тесты Т.А. Боровских 8 класс
издательство: УМК Экзамен
автор: Т.А. Боровских
ГДЗ по химии для 8 класса на 5.
 fun
fun- Химия 8 класс
- Авторы: Гузей Л.С., Суровцева Р.П., Сорокин В.В.
- Издательство: Дрофа 2002
- Химия 8 класс
- Автор: О.С. Габриелян
- Издательство: Дрофа 2015
- Химия 8 класс Дидактические материалы
- Автор: А.
 М. Радецкий
М. Радецкий - Издательство: Просвещение 2016
- Химия 8 класс
- Авторы: Г.Е. Рудзитис, Ф.Г. Фельдман
- Издательство: Просвещение 2015
- Химия 8 класс Задачник
- Авторы: Гольдфарб Я.
 Л., Ходаков Ю.В., Додонов Ю.Б.
Л., Ходаков Ю.В., Додонов Ю.Б. - Издательство: Дрофа 2004
- Химия 8 класс Сборник задач и упражнений
- Автор: Хомченко И.Г.
- Издательство: Новая волна 2009
- Химия 8 класс Задачник
- Авторы: Н.
 Е. Кузнецова, А.Н. Левкин
Е. Кузнецова, А.Н. Левкин - Издательство: Вентана-граф
- Химия 8 класс Рабочая тетрадь
- Авторы: В.В. Еремина, Н.Е. Кузьменко, А.А. Дроздова, В.В. Лунина
- Издательство: Дрофа 2016
- Химия 8 класс Задачник с помощником
- Авторы: Н.
 Н. Гара, Н.И. Габрусева
Н. Гара, Н.И. Габрусева - Издательство: Просвещение 2015
- Химия 8 класс
- Авторы: И.И. Новошинский, Н.С. Новошинская
- Издательство: Русское слово 2015
- Химия 8 класс Алгоритм успеха
- Авторы: Кузнецова Н.
 Е., Титова И.М., Гара Н.Н.
Е., Титова И.М., Гара Н.Н. - Издательство: Вентана-граф 2015
- Химия 8 класс Рабочая тетрадь
- Автор: Габрусева Н.И.
- Издательство: Просвещение 2016
- Химия 8 класс Тетрадь для оценки качества знаний
- Авторы: О.
 С. Габриелян, А.В. Купцова
С. Габриелян, А.В. Купцова - Издательство: Дрофа 2016-2018
- Химия 8 класс
- Авторы: Оржековский П. А., Мещерякова Л. М.
- Издательство: Аст/Астрель 2016
- Химия 8 класс
- Авторы: Еремин В.
 В., Кузьменко Н.Е., Дроздов А.А.
В., Кузьменко Н.Е., Дроздов А.А. - Издательство: Дрофа 2016
- Химия 8 класс
- Авторы: Минченков Е.Е., Журин А.А., Оржековский П.А.
- Издательство: Мнемозина 2013
- Химия 8 класс Рабочая тетрадь
- Авторы: Гара Н.
 Н., Ахметов М.А.
Н., Ахметов М.А. - Издательство: Вентана-граф 2017
- Химия 8 класс Сферы
- Автор: Журин А.А.
- Издательство: Просвещение 2016
- Химия 8 класс Тетрадь-тренажёр Сферы
- Автор: Гара Н.
 Н.
Н. - Издательство: Просвещение 2017
- Химия 8 класс Тетрадь-практикум Сферы
- Автор: Журин А.А,
- Издательство: Просвещение 2016
- Химия 8 класс Тетрадь-экзаменатор Сферы
- Авторы: Бобылева О.
 Л., Бирюлина Е.В., Дмитриева Е.Н.
Л., Бирюлина Е.В., Дмитриева Е.Н. - Издательство: Просвещение 2016
- Химия 8 класс
- Авторы: Шиманович И.Е., Красицкий В.А., Сечко О.И., Хвалюк В.Н.
- Издательство: Народная асвета 2018
- Химия 8 класс Сборник контрольных и самостоятельных работ
- Авторы: Масловская Т.
 Н., Пашуто Е.Н., Власовец Е.Н.
Н., Пашуто Е.Н., Власовец Е.Н. - Издательство: Аверсэв 2016
- Химия 8 класс Сборник задач УМК
- Автор: Рябов М.А.
- Издательство: Экзамен 2017
- Химия 8 класс
- Авторы: Габриелян О.
 С., Остроумов И.Г., Сладков С.А.
С., Остроумов И.Г., Сладков С.А. - Издательство: Просвещение 2018
- Химия 8 класс Контрольно-измерительные материалы (КИМ)
- Авторы: Троегубова Н.П., Стрельникова Е.Н.
- Издательство: ВАКО 2018
- Химия 8 класс Рабочая тетрадь
- Авторы: Габриелян О.
 С., Сладков С.А.
С., Сладков С.А. - Издательство: Дрофа 2018
- Химия 8 класс Контрольные и самостоятельные работы УМК
- Автор: Павлова Н.С.
- Издательство: Экзамен 2016
- Химия 8 класс
- Авторы: Усманова М.
 Б., Сакарьянова К.Н., Сахариева Б.Н.
Б., Сакарьянова К.Н., Сахариева Б.Н. - Издательство: Атамұра 2018
- Химия 8 класс Тетрадь для практических работ и лабораторных опытов
- Авторы: Габриелян О.С., Купцова А.В.
- Издательство: Дрофа 2018
- Химия 8 класс
- Авторы: Журин А.
 А., Корнилаев С.В., Шалашова М.М.
А., Корнилаев С.В., Шалашова М.М. - Издательство: Академкнига 2012
- Химия 8 класс Контрольные работы
- Авторы: Габриелян О.С., Краснова В.Г.
- Издательство: Дрофа 2017
- Химия 8 класс Контрольные и проверочные работы
- Авторы: Габриелян О.
 С., Березкин П.Н., Ушакова А.А.
С., Березкин П.Н., Ушакова А.А. - Издательство: Дрофа 2016
- Химия 8 класс Рабочая тетрадь УМК
- Автор: Боровских Т.А.
- Издательство: Экзамен 2018
- Химия 8 класс Задачник Сферы
- Автор: Журин А.
 А.
А. - Издательство: Просвещение 2019
- Химия 8 класс Рабочая тетрадь
- Авторы: Габриелян О.С., Остроумов И.Г., Сладков С.А.
- Издательство: Просвещение 2020
- Химия 8 класс Тесты
- Автор: М.
 А. Рябов
А. Рябов - Издательство: Экзамен 2016
- Химия 8 класс Тесты
- Автор: М.А. Рябов
- Издательство: Экзамен 2015
- Химия 8 класс Тесты УМК
- Автор: Т.
 А. Боровских
А. Боровских - Издательство: Экзамен 2013
- Химия 8 класс Сборник задач
- Автор: Маршанова Г.Л.
- Издательство: ВАКО 2019
- Химия 8 класс Сборник контрольных и самостоятельных работ
- Авторы: Сеген Е.
 Л., Власовец Е.Н., Гарбар Е.Е., Синявская Т.С.
Л., Власовец Е.Н., Гарбар Е.Е., Синявская Т.С. - Издательство: Аверсэв 2020
- Химия 8 класс Рабочая тетрадь УМК
- Автор: Микитюк А.Д.
- Издательство: Экзамен 2015
- Химия 8 класс Проверочные и контрольные работы
- Авторы: Габриелян О.
 С., Лысова Г.Г.
С., Лысова Г.Г. - Издательство: Просвещение 2021
- Химия 8 класс Контрольные измерительные материалы Контрольные измерительные материалы
- Авторы: Корощенко А.С., Яшукова А.В.
- Издательство: Экзамен 2016
- Химия 8 класс Тетрадь для практических работ и лабораторных опытов
- Авторы: О.
 С. Габриелян, И.В. Аксенова, И.Г. Остроумов
С. Габриелян, И.В. Аксенова, И.Г. Остроумов - Издательство: Просвещение 2020
- История 8 класс
- Авторы: А.Я. Юдовская, П.А. Баранов, Л.М. Ванюшкина
- Издательство: Просвещение 2014-2019
- Геометрия 8 класс
- Авторы: Л.
 С. Атанасян, В.Ф. Бутузов, С.Б. Кадомцев, Э.Г. Позняк, И.И. Юдин
С. Атанасян, В.Ф. Бутузов, С.Б. Кадомцев, Э.Г. Позняк, И.И. Юдин - Издательство: Просвещение
- Английский язык 8 класс Forward
- Авторы: Вербицкая М.В., Маккинли С., Хастингс Б., Миндрул О.С.
- Издательство: Вентана-граф 2016
- География 8 класс
- Авторы: В.
 П. Дронов, И. И. Баринова, В. Я. Ром, А. А. Лобжанидзе
П. Дронов, И. И. Баринова, В. Я. Ром, А. А. Лобжанидзе - Издательство: Дрофа 2014
- История 8 класс Рабочая тетрадь
- Авторы: Юдовская А. Я., Ванюшкина Л. М., Баранов П. А.
- Издательство: Просвещение 2016-2020
- Физика 8 класс Классический курс
- Авторы: Громов С.
 В., Родина Н.А., Белага В.В., Ломаченков И.А., Панебратцев Ю.А.
В., Родина Н.А., Белага В.В., Ломаченков И.А., Панебратцев Ю.А. - Издательство: Просвещение 2018
- География 8 класс Полярная звезда
- Авторы: А. И. Алексеев, В. В. Николина, Е. К. Липкина
- Издательство: Просвещение 2016
- Русский язык 8 класс Школа 2100
- Авторы: Бунеев Р.
 Н., Бунеева Е.В., Комиссарова Л.Ю., Текучева И.В.
Н., Бунеева Е.В., Комиссарова Л.Ю., Текучева И.В. - Издательство: Баласс 2016
- Английский язык 8 класс
- Авторы: В.П. Кузовлев, Н.М. Лапа, Э.Ш. Перегудова
- Издательство: Просвещение 2015
ГДЗ по химии для 8 класса от Спиши фан
Сборник Задач по химии 8 класс В.
 Н. Хвалюк
Н. ХвалюкАвторы: В.Н. Хвалюк, В.И. Резяпкин
Задачник С Помощником по химии 8 класс Н.Н. Гара
Авторы: Н.Н. Гара, Н.И. Габрусева
Рабочая Тетрадь по химии 8 класс О.И. Сечко
Авторы: О.И. Сечко, И.Е. Шиманович
Задачник по химии 8 класс Гольдфарб Я.Л.
Авторы: Гольдфарб Я.Л., Ходаков Ю.В., Додонов Ю.Б.
Решебник по химии 8 класс Кузнецова Н.
 Е.
Е.Авторы: Кузнецова Н.Е., Титова И.М., Гара Н.Н.
Решебник по химии 8 класс Г.Е. Рудзитис
Авторы: Г.Е. Рудзитис, Ф.Г. Фельдман
Рабочая Тетрадь по химии 8 класс Габрусева Н.И.
Автор: Габрусева Н.И.
Тетрадь Для Практических Работ И Лабораторных Опытов по химии 8 класс О.И. Сечко
Автор: О.И. Сечко
Решебник по химии 8 класс Минченков Е.
 Е.
Е.Авторы: Минченков Е.Е., Журин А.А., Оржековский П.А.
Решебник по химии 8 класс Л.С. Гузей
Автор: Л.С. Гузей
Решебник по химии 8 класс Оржековский П. А.
Авторы: Оржековский П. А., Мещерякова Л. М.
Решебник по химии 8 класс И.И. Новошинский
Авторы: И.И. Новошинский, Н.С. Новошинская
Дидактические Материалы по химии 8 класс А.
 М. Радецкий
М. РадецкийАвтор: А.М. Радецкий
Решебник по химии 8 класс Шиманович И.Е.
Авторы: Шиманович И.Е., Красицкий В.А., Сечко О.И., Хвалюк В.Н.
Рабочая Тетрадь по химии 8 класс В.В. Еремина
Авторы: В.В. Еремина, Н.Е. Кузьменко, А.А. Дроздова, В.В. Лунина
Тетрадь Для Практических Работ И Лабораторных Опытов по химии 8 класс И.И. Борушко
Автор: И.И. Борушко
- org/Book»>
Сборник Задач И Упражнений по химии 8 класс Хомченко И.Г.
Автор: Хомченко И.Г.
Задачник по химии 8 класс Н.Е. Кузнецова
Авторы: Н.Е. Кузнецова, А.Н. Левкин
Решебник по химии 8 класс О.С. Габриелян
Автор: О.С. Габриелян
Тетрадь Для Оценки Качества Знаний по химии 8 класс О.С. Габриелян
Авторы: О.С. Габриелян, А.В. Купцова
- org/Book»>
Рабочая Тетрадь по химии 8 класс Гара Н.Н.
Авторы: Гара Н.Н., Ахметов М.А.
Решебник по химии 8 класс Журин А.А.
Автор: Журин А.А.
Тетрадь-Тренажёр по химии 8 класс Гара Н.Н.
Автор: Гара Н.Н.
Решебник по химии 8 класс Еремин В.В.
Авторы: Еремин В.В., Кузьменко Н.Е., Дроздов А.А.
Тетрадь-Практикум по химии 8 класс Журин А.
 А,
А,Автор: Журин А.А,
Тетрадь-Экзаменатор по химии 8 класс Бобылева О.Л.
Авторы: Бобылева О.Л., Бирюлина Е.В., Дмитриева Е.Н.
Сборник Контрольных И Самостоятельных Работ по химии 8 класс Масловская Т.Н.
Авторы: Масловская Т.Н., Пашуто Е.Н., Власовец Е.Н.
Сборник Задач по химии 8 класс Рябов М.А.
Автор: Рябов М.А.
Решебник по химии 8 класс Габриелян О.
 С.
С.Авторы: Габриелян О.С., Остроумов И.Г., Сладков С.А.
Контрольно-Измерительные Материалы (Ким) по химии 8 класс Троегубова Н.П.
Авторы: Троегубова Н.П., Стрельникова Е.Н.
Рабочая Тетрадь по химии 8 класс Габриелян О.С.
Авторы: Габриелян О.С., Сладков С.А.
Контрольные И Самостоятельные Работы по химии 8 класс Павлова Н.С.
Автор: Павлова Н.С.
- org/Book»>
Тетрадь Для Практических Работ И Лабораторных Опытов по химии 8 класс Габриелян О.С.
Авторы: Габриелян О.С., Купцова А.В.
Решебник по химии 8 класс Журин А.А.
Авторы: Журин А.А., Корнилаев С.В., Шалашова М.М.
Контрольные Работы по химии 8 класс Габриелян О.С.
Авторы: Габриелян О.С., Краснова В.Г.
Решебник по химии 8 класс Усманова М.Б.
Авторы: Усманова М.Б., Сакарьянова К.Н., Сахариева Б.Н.
- org/Book»>
Рабочая Тетрадь по химии 8 класс Боровских Т.А.
Автор: Боровских Т.А.
Задачник по химии 8 класс Журин А.А.
Автор: Журин А.А.
Рабочая Тетрадь по химии 8 класс Габриелян О.С.
Авторы: Габриелян О.С., Остроумов И.Г., Сладков С.А.
Контрольные И Проверочные Работы по химии 8 класс Габриелян О.С.
Авторы: Габриелян О.С., Березкин П.Н., Ушакова А.А.
- org/Book»>
Решебник по химии 8 класс Савчин М.М.
Автор: Савчин М.М.
Решебник по химии 8 класс О.Г. Ярошенко
Автор: О.Г. Ярошенко
Решебник по химии 8 класс П.П. Попель
Авторы: П.П. Попель, Л.С. Крикля
Рабочая Тетрадь по химии 8 класс Савчин М.М.
Автор: Савчин М.М.
Решебник по химии 8 класс Н.
 М. Буринськая
М. БуринськаяАвтор: Н.М. Буринськая
Решебник по химии 8 класс Григорович О.В.
Автор: Григорович О.В.
Решебник по химии 8 класс Лашевська Г.А.
Авторы: Лашевська Г.А., Лашевська А.А.
Решебник по химии 8 класс Гранкина Т.М.
Автор: Гранкина Т.М.
Решебник по химии 8 класс Дячук Л.С.
Авторы: Дячук Л.
 С., Гладюк М.М.
С., Гладюк М.М.Рабочая Тетрадь по химии 8 класс Иванащенко О.А.
Авторы: Иванащенко О.А., Михайлова И.Г., Путников А.В.
Тесты по химии 8 класс М.А. Рябов
Автор: М.А. Рябов
Тесты по химии 8 класс М.А. Рябов
Автор: М.А. Рябов
Тесты по химии 8 класс Т.А. Боровских
Автор: Т.А. Боровских
org/Book»>Сборник Контрольных И Самостоятельных Работ по химии 8 класс Сеген Е.Л.
Авторы: Сеген Е.Л., Власовец Е.Н., Гарбар Е.Е., Синявская Т.С.
Рабочая Тетрадь по химии 8 класс Микитюк А.Д.
Автор: Микитюк А.Д.
Сборник Задач по химии 8 класс Маршанова Г.Л.
Автор: Маршанова Г.Л.
Проверочные И Контрольные Работы по химии 8 класс Габриелян О.С.
Авторы: Габриелян О.С., Лысова Г.Г.
org/Book»>Тетрадь Для Практических Работ И Лабораторных Опытов по химии 8 класс О.С. Габриелян
Авторы: О.С. Габриелян, И.В. Аксенова, И.Г. Остроумов
Контрольные Измерительные Материалы по химии 8 класс Корощенко А.С.
Авторы: Корощенко А.С., Яшукова А.В.
8 лучших учебников по химии
Обновлено: 14.03.2019 11:22:30
Эксперт: Анфиса Вернер
С 8 класса в школах начинают изучать химию. К учебникам по этому предмету предъявляется довольно много требований. Наши специалисты выяснили, какое учебное пособие по дисциплине считают преподаватели и студенты лучшими. При составлении рейтинга учитывались следующие факторы:
- последовательность представленного материала;
- высококачественных определений транскриптов;
- наличие тестовых упражнений и заданий разной сложности;
- наличие в комплекте рабочей тетради для учителя, тетрадей для школьников.

Каждый из представленных учебников имеет свои особенности подачи информации. Стоит познакомиться с ними поближе.
Рейтинг лучших учебников по химии
| Номинация | место | учебник | рейтинг |
| Лучшие учебники по химии российских авторов | 1 | Химия. 9 класс. Учебник. Гузей Л.С. и др. | 4.9 |
| 2 | Н. Е. Кузнецова Химия 8 класс | 4,8 | |
| 3 | О. С. Габриелян Учебник химии для 8 класса | 4.7 | |
| 4 | Е. Е. Минченков Общая методика обучения химии | 4.6 | |
| 5 | Химия. 9 класс. Шелинский и Юрова | 4,5 | |
| Лучшие учебники по химии зарубежных авторов | 1 | Фримантл М. Химия в действии. Часть 1 Химия в действии. Часть 1 | 4.9 |
| 2 | Неорганическая химия, том первый, Шрайвер, Аткинс, | 4,8 | |
| 3 | Аналитическая химия. Проблемы и подходы. Том 1. Под ред. Р. Кельнер, Ж.-М. Мерме, М. Отто. | 4.7 |
Лучшие учебники по химии российских авторов
Авторы отразили в своей работе неоспоримую роль химии и ее влияние на жизнь человека. Активное развитие науки в 20 веке послужило толчком к созданию многих популярных учебников.
Химия. 9 класс. Учебник. Гузей Л.С. и др.
Рейтинг: 4,9
На вершине рейтинга находится двухуровневое пособие для девятого класса. В издание включены материалы, направленные на углубленное изучение темы. В книге изложены новые достижения науки, предложены актуальные методы обучения. Вместе с учебником предоставляются рабочие тетради, методические пособия для учителя. Примечательно, что учебник начинается с раздела «Вспомним прошлый год». Следующее обсуждение посвящено жидким, атомарным и молекулярным кристаллам.
Примечательно, что учебник начинается с раздела «Вспомним прошлый год». Следующее обсуждение посвящено жидким, атомарным и молекулярным кристаллам.
Преподаватели в восторге от четкой подачи материала, при которой необходимость заучивания информации сведена к минимуму. Учащийся начинает осознавать суть практического применения знаний. Это облегчает задачу учителя. Именно поэтому книга – лучший вариант для начинающих.
Кузнецова Н.Е. Химия 8 класс
Рейтинг: 4,8
Следующего участника рейтинга ценят многие педагоги. В этом учебнике органическая химия доходчиво и правильно изложена. Радует информация, доступная для школьных умов, отдельный раздел с методами современной науки. В тексте представлены различные работы на практике и лабораторные эксперименты. В конце абзацев предлагаются задания, в том числе и творческие.
Автор пособия – доктор педагогических наук. Кузнецова правильно и правильно отобразила материал, который носит исследовательский характер. Содержание книги мотивирует учебную деятельность и объединяет знания по физике, химии и биологии. Пособие побуждает к поиску информации и изучению дисциплины в будущем. Язык учебника понятен и научен. Таким образом, 8 класс по химии полностью соответствует личным и предметным требованиям.
Содержание книги мотивирует учебную деятельность и объединяет знания по физике, химии и биологии. Пособие побуждает к поиску информации и изучению дисциплины в будущем. Язык учебника понятен и научен. Таким образом, 8 класс по химии полностью соответствует личным и предметным требованиям.
Габриелян О.С. Учебник химии для 8 класса
Рейтинг: 4,7
В рамках курса восьмого класса предлагается методическое пособие Габриеляна. Автор книги – профессор, заслуженный учитель Российской Федерации. Учебник соответствует государственному стандарту образования. Ученикам нравятся красочные рисунки, интересные задания и разные вопросы. Все они способствуют активному усвоению материала.
Сейчас этим пособием пользуются многие классы. Он содержит ясность и смысл информации. Здесь подробно обсуждаются химические вещества, а на форзаце отображается периодическая таблица. Из недостатков можно отметить несоответствие заданий возрасту учащихся. Некоторые формулировки приходится запоминать.
Минченков Е.Е. Общая методика обучения химии
Рейтинг: 4,6
Автор данного учебника предлагает поверхностное и углубленное изучение тем. Такой подход удобен тем, что школьники лучше воспринимают информацию и усваивают сложные химические термины. Особую роль играет практический эксперимент. В учебнике правильно подобран теоретический материал, есть много примеров, поясняющих изложенную выше информацию. Текст свободно воспринимается подростками. Вопросы и задания помогают закрепить материал, сконцентрироваться на главном.
Это пособие охватывает больше тем, чем другие учебники. Все, что написано, подкреплено аргументами. Прочитал публикацию с большим интересом. Отзывы о нем в основном положительные. Книгу трудно найти в печатной версии, но она широко доступна в электронном виде.
Химия. 9 класс. Шелинский и Юрова
Рейтинг: 4,5
Завершает рейтинг руководство, которое познакомит учащихся с видами металлов, возможностью их использования в различных сферах жизни. В этой книге учащиеся узнают о природе химических связей, строении объектов, теории растворов проводников второго рода и др. В конце курса учащиеся найдут сокращенное изложение химии органических элементов .
В этой книге учащиеся узнают о природе химических связей, строении объектов, теории растворов проводников второго рода и др. В конце курса учащиеся найдут сокращенное изложение химии органических элементов .
Автор пособия — преподаватель химического факультета ЛИТМО, участник ВОВ, главный инженер химического завода, кандидат педагогических наук. В 2010 году профессор Шелинский умер, но по его книгам многие студенты до сих пор занимаются для того, чтобы расширить кругозор. Учителя обращаются к его учебникам по химии, если хотят глубже вникнуть в материал, лаконично изложенный в других книгах.
Лучшие учебники по химии зарубежных авторов
Во всех развитых странах изучение химии занимает особое место. В России эта наука только начинает набирать популярность. Поэтому всем тем, кто хочет пополнить свои знания в области данной области, необходимо ознакомиться с работами европейских ученых, считающих химию областью будущего.
Фримантл М. Химия в действии.
 Часть 1
Часть 1Рейтинг: 4,9
Пособие Фримантл в двух томах отлично подойдет для подготовки к ЕГЭ. Он позволяет заполнять интервалы в школьной программе. Это отличный выбор для студентов-химиков. Весь материал отображается простым и доступным языком. В ней есть вся необходимая информация о современной науке. В учебнике нет неподтвержденной теории. В него включены исторические данные, выдержки из популярных изданий, множество примеров и фотографий. В книге представлены схематические таблицы и графики. Темы выложены в стандартной последовательности.
Стоит учесть, что с 1998 года учебник не издается. Его можно найти в библиотеках, в электронной онлайн-версии. Встречается в магазинах, специализирующихся на вторичной торговле печатными изданиями.
Неорганическая химия, том первый, Шрайвер, Аткинс
Рейтинг: 4,8
Далее в рейтинге ценное издание по неорганической химии, составленное экспертами из Америки и Великобритании. Авторы занимаются просветительской деятельностью. В своей книге они подробно рассматривают положения теории, в том числе модели химических связей, теорию кислот. Особое внимание уделено актуальным проблемам науки.
Авторы занимаются просветительской деятельностью. В своей книге они подробно рассматривают положения теории, в том числе модели химических связей, теорию кислот. Особое внимание уделено актуальным проблемам науки.
Учебник прекрасно иллюстрирован и содержит богатый справочный материал, множество заданий разной сложности. Книга издана на русском языке в двух частях. Это хороший выбор для студентов и преподавателей химических факультетов, который позволит расширить свои знания.
Аналитическая химия. Проблемы и подходы. Том 1. Под ред. Р. Кельнер, Ж.-М. Мерме, М. Отто.
Рейтинг: 4,7
Последний учебник был создан авторитетными учеными из организации научной деятельности в Европе. Рекомендуется в качестве основного пособия по основам химического анализа для студентов и преподавателей вузов. Темы: компьютерные технологии, хемометрика, физические методы анализа, технологии управления технологическими процессами и др.
На русском языке пособие издано в двух томах под руководством а. с. Золотов. Он доступен в Интернете для скачивания. Отзывы о нем в основном одобрительные. Это отличный вариант для тех, кто увлечен химией и хочет связать свою жизнь с этой наукой.
с. Золотов. Он доступен в Интернете для скачивания. Отзывы о нем в основном одобрительные. Это отличный вариант для тех, кто увлечен химией и хочет связать свою жизнь с этой наукой.
Внимание! Данный рейтинг субъективен, не является рекламой и не служит ориентиром при покупке. Перед покупкой следует проконсультироваться со специалистом.
Комментарии
Урок 1 по химии. Как сделать урок химии интересным
8 класс
Урок 1
«Предмет химии»
Цели урока. Образовательная: познакомить учащихся с предметом химии; дать представление о химии как о точной науке, не лишенной лирики; представить точки зрения на происхождение слова «химия»; показать связь химии с другими науками.
Развивающие: развитие познавательного интереса к предмету; ознакомление учащихся с достижениями современной науки, с биографиями великих химиков.
Воспитательная: воспитание любви к Отечеству, гордости за достижения и успехи нашей страны в области науки; воспитание бережного отношения к своему здоровью; воспитание уважения к разным точкам зрения других людей.
Оборудование и реагенты.портреты Ж.Я. Берцелиус, Д. И. Менделеев, Р. Бунзен, Ф. А. Кекуле, Н. Н. Бекетов, С. Аррениус, Р. Вуд, Н. Н. Зинин; штативы с пробирками, химические стаканчики, тигельные щипцы, спиртовка, фарфоровый стаканчик, коническая колба, щепка; вода, раствор аммиака, раствор уксусной кислоты, спирт этиловый, бензин, соль, сахар, крахмал, мука, кубики льда, вата, песок речной, опилки, парафин, медный купорос, железные опилки, медная стружка, фосфор красный, сера, КИ растворы, Pb(NO 3 ) 2 , КОН, CuSO 4 , NaOH, FeCl 3 , Na 2 SO 4 , BaCl 2 , HCl, Na 2 CO 3 , CaCl 2 , лакмус, фенолфталеин, дихромат аммония.
1. Организационное время.
Введение в класс.
2. Актуализация знаний.
Какие ассоциации у вас вызывает слово «химия»?
К какой группе наук относится химия?
Вы уже знаете, как переводятся слова: «география», «геометрия», «биология», а как переводится слово «химия»?
3. Информация.
Существует несколько точек зрения на происхождение слова «химия».
а) Хми (египетское) – «черная» земля. древнее название Египта, где зародилась наука химия.
б) Кеме (египетское) — «черная» наука. Алхимия как темная, дьявольская наука (сравните с черной книгой — колдовством, основанным на действии злых духов).
в) Хума (др.-греч.) — «отливка» металлов; тот же корень и у греческого humos — «сок».
г) Ким (др.-кит.) – «золото». Тогда химию можно интерпретировать как «изготовление золота».
4. Разминка.
Хоть химия и сложная наука, но вы уже многое знаете из других наук, из жизненного опыта. Сами увидим: вам предлагаются вопросы из различных тем курса химии 8, 9, 10 классов. Кто хочет ответить?
Вопросы викторины «Действительно ли это сложная химия?»
Почему мы дуем на спичку, когда хотим ее потушить?
(Выдыхаемый воздух содержит CO 2 .)
Почему горящий бензин нельзя потушить водой?
(Бензин легче воды и не смешивается с ней.)
Как носить 1 литр воды на ладони, не пролив ни капли?
(Заморозить во льду. )
)
Что теплее: три рубашки или тройная рубашка?
(Три рубашки.)
В каком море нельзя утонуть? Почему?
(На Мертвом море очень соленое.)
Что тяжелее: 1 кг железа или 1 кг хлопка?
(Они равны.)
Из 1 г какого металла можно вытянуть проволоку длиной 2,5 км?
(Из золота.)
Можно ли заполнить воздухом только половину шара?
(Запрещено.)
Что означает выражение «вода с гуся»?
(Перья водоплавающих птиц не смачиваются водой.)
Соединения каких металлов придают планете Марс красный оттенок?
(Соединения железа.)
Три одинаковые горящие свечи были одновременно накрыты тремя банками емкостью 0,4 л, 0,6 л и 1 л. Что случится?
(Свеча погаснет тем раньше, чем меньше объем банки.)
Так что же такое химия?
Химия — это наука о веществах, их свойствах, превращениях и явлениях, сопровождающих эти превращения
Вещество — это то, из чего состоит тело.
Тело – ограниченная в пространстве часть материи.
Упражнение:
- Из приведенного ниже списка определите вещество или тело:
гвоздь, стекло, стекло, воронка, железо, линейка, крахмал, алюминиевая проволока.
- Укажите вещества, из которых изготовлены корпуса:
подкова, вилка, линейка, пробирка, ручка
- О каких веществах можно сказать:
А) при нормальных условиях — бесцветная жидкость без вкуса, запаха, tкип = 100°С, твердеет при 0°С. Почему?
Б) красноватое твердое вещество, хорошо проводит электричество, обладает высокой пластичностью, позволяет изготавливать тонкую проволоку.
Итак, мы говорим с вами о свойствах веществ
Свойства — это признаки, по которым одни вещества отличаются от других или похожи друг на друга.
Свойства физические и химические.
Физические свойства — цвет, вкус, запах, агрегатное состояние, электро- и теплопроводность, температуры плавления и кипения, плотность.
5. Игра «Угадай вещество».
Что такое химия без экспериментов? Конечно, вы сами хотите «хим»! Знаете ли вы вещества? Вы можете отличить их друг от друга?
Проверим…
На демонстрационном столе учителя три лотка с веществами —
в одном бесцветная прозрачная жидкость,
в другом только белые твердые вещества,
в третьем, разноцветные твердые тела.
В е с е с т в а
1-й лоток. В маленьких стаканчиках: вода, раствор аммиака, раствор уксусной кислоты, спирт этиловый, бензин.
2-й лоток. Твердые вещества в стаканчиках белого цвета: соль, сахар, крахмал, мука, кубики льда, вата.
3-й лоток. В чашечках твердые разноцветные вещества: речной песок, опилки, парафин, медный купорос, железные опилки, медная стружка, красный фосфор, сера.
Нужны трое добровольцев в качестве экспериментаторов, которые попытаются определить предлагаемые вещества, обязательно объясняя свои действия.
Учитель предупреждает учащихся о соблюдении правил безопасности при проведении эксперимента.
Учащиеся пытаются идентифицировать вещества.
6. Информация. Интересные факты из жизни химиков.
Показаны портреты ученых.
Повар Берцелиуса.
Жители небольшого городка, в котором работал известный шведский ученый Дж.Дж. Берцелиус жил и работал однажды, спросил своего повара: «Чем, собственно, занимается ваш барин?»
– Точно не могу сказать, – ответила она, – берет большую фляжку с какой-то жидкостью, наливает в маленькую, встряхивает, наливает в еще меньшую, снова встряхивает и наливает в очень маленькую…»
«А потом?»
«А потом он все выливает!»
Демонстрация
Для опыта берутся 4 колбы разного объема. В большую колбу сначала наливают бесцветный раствор щелочи, колбу меньшего размера предварительно смачивают раствором фенолфталеина. Раствор щелочи приливают в колбу с фенолфталеином, раствор окрашивается в малиновый цвет. В третью колбу, еще меньшую, наливают немного раствора соляной кислоты большей концентрации, чем раствор щелочи, а затем в нее приливают окрашенный раствор щелочи. В третьей колбе раствор обесцвечивается. А когда всю смесь переливают в очень маленькую колбу, в которой находится немного концентрированного раствора щелочи, раствор снова приобретает малиновый цвет.
В третьей колбе раствор обесцвечивается. А когда всю смесь переливают в очень маленькую колбу, в которой находится немного концентрированного раствора щелочи, раствор снова приобретает малиновый цвет.
Мастер чемоданов.
Д.И.Менделеев любил переплетать книги, клеить рамы для портретов, мастерить чемоданы. Покупки для этих работ он обычно делал в Гостином дворе. Однажды, выбирая нужный товар, он услышал за спиной: «Кто этот почтенный господин?» — Таких людей надо знать, — с уважением в голосе ответил приказчик. «Это чемоданчик Менделеев!»
Хороший друг.
Однажды к Роберту Бунзену пришел коллега. Они разговаривали полтора часа. И гость уже собирался уходить, как вдруг Бунзен сказал: «Вы не представляете, как слаба моя память. Ведь когда я тебя увидел, то подумал, что ты Кекуле!» Посетитель посмотрел на него с изумлением и воскликнул: «Но я Кекуле!»
Сванте Аррениус.
Сванте Аррениус очень рано начал набирать вес. Он рассказал историю, связанную со своим лишним весом. Однажды ученые собрались в центральной гостинице Берлина для очередных дебатов. Аррениус оставил пальто в гардеробе и открыл дверь, чтобы присоединиться к коллегам, но гардеробщик остановил его словами: «Вы идете не туда, сэр, рядом сидит мясная корпорация!»
Однажды ученые собрались в центральной гостинице Берлина для очередных дебатов. Аррениус оставил пальто в гардеробе и открыл дверь, чтобы присоединиться к коллегам, но гардеробщик остановил его словами: «Вы идете не туда, сэр, рядом сидит мясная корпорация!»
На работе.
Американский физик Роберт Вуд начал свою карьеру лаборантом. Однажды его начальник зашел в комнату, наполненную грохотом и лязгом насосов и оборудования, и застал там Вуда, поглощенного чтением криминального романа. Возмущению вождя не было предела.
— Мистер Вуд! — воскликнул он, воспылав гневом, — вы… вы позволяете себе читать детектив?!
— Ради бога, прости! Вуд был в замешательстве. — Но с таким шумом поэзия просто не воспринимается!
Героические забавы профессора Зинина.
Применялось ли насилие в отношении студентов в России? Грубого насилия не было, но учителя, хотя и редко, применяли наручники. Известный академик Н.Н. Зинин не только ругал нерадивых учеников, но и бил их. Никто на это не обиделся, т.к. было разрешено дать сдачу академику. Но охотников для принятия ответных мер не нашлось. Зинин обладал большой физической силой и мог так сжать противника в объятиях, что тот долго не мог прийти в себя.
Никто на это не обиделся, т.к. было разрешено дать сдачу академику. Но охотников для принятия ответных мер не нашлось. Зинин обладал большой физической силой и мог так сжать противника в объятиях, что тот долго не мог прийти в себя.
7. Чудеса своими руками.
На столах учеников стоят стойки с двумя пробирками.
Вы сами отличные экспериментаторы, с помощью нехитрых трюков можно творить чудеса. Ваша задача смешать содержимое пробирок между собой.
Учитель объясняет ученикам правила безопасности эксперимента.
Растворы подобраны таким образом, что в каждом случае либо выпадают осадки разного цвета, либо выделяется газ, либо изменяется цвет.
Студенты проводят эксперимент, наблюдают за происходящими изменениями. (Например, растворы йодистого калия и нитрата свинца (II); гидроксида калия и сульфата меди (II); гидроксида натрия и хлорида железа (III); сульфата натрия и хлорида бария; лакмуса и соляной кислоты, лакмуса и гидроксида натрия; уксусной кислоты. кислота и карбонат натрия и др.)
кислота и карбонат натрия и др.)
8. Поиграем…
Игра «Угадай что?»
Первым делом
1) Это вещество в старину называли владыкой жизни и смерти. Его приносили в жертву богам, а иногда и поклонялись как божеству.
(5 баллов.)
2) Служил мерилом богатства, могущества, выносливости, могущества, считался хранителем молодости и красоты.
(4 балла.)
3) По поверьям имеет способность помогать человеку во всех его делах, уберегать от бед и напастей.
(3 балла.)
4) «Он родится из воды, но воды боится».
(2 балла)
5) Широко используется в быту, в кулинарии, в кожевенном деле, в текстильной промышленности и др.
(1 балл)
(Ответ. Соль.)
Секунда
1) Древние египтяне называли его «vaaepere», что означает «рожденный в небе».
(5 баллов)
2) Древние копты называли его «камнем неба».
(4 балла.)
3) Изделия из него ценились дороже золота. Кольца и броши из него могли делать только очень богатые люди.
(3 балла.)
4) Алхимики считали его настолько неблагородным металлом, что с ним не стоило иметь дело.
(2 балла)
5) Его именем назван век. Это пластичный мягкий металл.
(1 балл)
(Ответ. Железо.)
9. «Знаете ли вы, что…»
Учитель. Сейчас мы узнаем о достижениях современной науки, об интересных открытиях в области химии и смежных наук.
Нано (от греческого nanos — карлик) — миллиардная часть чего-либо. Область науки, изучающая свойства объектов размером 10–9м. Нанотехнологии манипулируют отдельными частицами размером от 1 до 100 нм, а также разрабатывают устройства подобных размеров. Сейчас созданы порошки и суспензии, улучшающие работу двигателей и механизмов. Покрытия из материалов, изготовленных с использованием нанотехнологий, предотвращают появление ржавчины, помогают материалу самоочищаться или не смачиваться водой. Первые нанороботы способны путешествовать по телам животных. Водород можно безопасно хранить с помощью нанотрубок. В будущем можно конструировать любые молекулы и создавать сверхпрочные материалы. В медицине планируется создание таргетных препаратов, проникающих в пораженную ткань или опухоль; использование нанороботов для диагностики и лечения практически всех заболеваний, выращивание тканей и органов. В электронике это создание сверхминиатюрных электронных устройств, гибких дисплеев, электронной бумаги, новых типов двигателей и топливных элементов.
В будущем можно конструировать любые молекулы и создавать сверхпрочные материалы. В медицине планируется создание таргетных препаратов, проникающих в пораженную ткань или опухоль; использование нанороботов для диагностики и лечения практически всех заболеваний, выращивание тканей и органов. В электронике это создание сверхминиатюрных электронных устройств, гибких дисплеев, электронной бумаги, новых типов двигателей и топливных элементов.
Многие гляциологи считают, что толщина полярных ледяных щитов неуклонно сокращается. За 5 лет объем льда, сходящего в Атлантику ежегодно, увеличился почти в 2 раза, что эквивалентно подъему уровня Мирового океана на 0,5 мм в год. Антарктида в период с 2002 по 2005 год ежегодно теряла в среднем 152 км 3 лед. Уровень океана к 2100 г. может подняться на 4–6 м от современного уровня.
Греческие и латинские надписи, сделанные на камнях 2000 лет назад, не читаются из-за разрушившей их эрозии. Для восстановления надписей ученые использовали флуоресцентный метод: при бомбардировке поверхности рентгеновскими лучами атомы возбуждаются, а затем, возвращаясь в состояние покоя, излучают видимый свет. Это позволяет определить следы свинца или железа, оставленные резцом античного автора.
Это позволяет определить следы свинца или железа, оставленные резцом античного автора.
Российские химики придумали, как перерабатывать пластиковые бутылки, а также синтезировали новый наполнитель для каучуков и полимеров. Водородное топливо вместо выхлопных газов даст чистую воду.
В США разработано прозрачное полимерное настенное покрытие, к которому ничего не прилипает. Это разновидность тефлона. На таком покрытии невозможно писать или рисовать красками, мелом или фломастером. Покрытие может быть использовано для защиты днищ морских судов от обрастания и фюзеляжей самолетов от обледенения.
10. Развлекательные демонстрационные опыты.
Учитель. Сегодня было ваше первое знакомство с химией. Конечно, вас ждет что-то необычное, чудесное. Я постараюсь превратиться в волшебника и показать вам чудеса химии.
Учитель демонстрирует опыты.
«Дым без огня».
Две чашки смачивают концентрированными растворами нашатырного спирта и соляной кислоты, а затем подносят друг к другу. Обратите внимание на дым без огня.
Обратите внимание на дым без огня.
«Из одного стакана — газированная вода, малиновый сок и молоко».
Бесцветные прозрачные растворы соляной кислоты, хлористого кальция и фенолфталеина наливают в три одинаковых стакана. Налейте раствор карбоната натрия в фарфоровую кружку. Затем карбонат натрия выливают из кружки по очереди в каждый из трех стаканов. В первом из них быстро выделяется газ («газировка»), во втором появляется белый осадок («молочный»), а в третьем раствор приобретает малиновый цвет из-за изменения цвета индикатора в щелочной раствор («малиновый сок»).
«Огнеупорный шарф».
Платок замачивают в воде, а затем в этиловом спирте. С помощью тигельных щипцов его подносят к горящей спиртовке и поджигают. Несмотря на огромное пламя, платок в итоге остается целым, т.к. спирт воспламеняется и сгорает раньше, чем воспламеняется влажная тряпка.
Вулкан на столе.
На горлышко конической колбы помещают фарфоровую чашку. Под колбу кладут большой лист бумаги. Дихромат аммония наливают в чашку, слегка смоченную в центре спиртом. «Вулкан» горит осколком. Реакция протекает бурно, создается впечатление извергающегося вулкана, из кратера которого изливаются раскаленные массы.
Дихромат аммония наливают в чашку, слегка смоченную в центре спиртом. «Вулкан» горит осколком. Реакция протекает бурно, создается впечатление извергающегося вулкана, из кратера которого изливаются раскаленные массы.
11. Подведение итогов урока.
Д/з: §- 1-я стр. 13 №3,4
Урок разработан для УМК Г.Е. Рудзитис, Ф.Г. Фельдман.
Основная цель данного занятия — обобщить и закрепить знания учащихся по начальным химическим понятиям; активизация познавательной деятельности и повышение мотивации учащихся к изучению химии. Развитие интереса учащихся к химии и активизация их познавательной деятельности, с использованием нестандартных игровых форм учебной деятельности. Занятие проводится в форме турнира.
На уроке используются ИКТ, необходимость использования компьютерной презентации продиктована следующими причинами:
- Организация разнообразной деятельности учащихся.
- Средства для обеспечения видимости и уплотнения материала.
- Организация самопроверки без затрат времени урока.

- Помогает сэкономить время занятий
Методы: словесный, наглядный, с использованием ИКТ, проблемно-поисковый.
Цели игры:
- повторение изученного материала по химии для заполнения пропусков и подготовки к плановой контрольной работе;
- развитие и укрепление интереса к химии, расширение кругозора учащихся, повышение уровня их культуры;
- развитие коммуникативных навыков, уверенности и раскованности в общении;
- воспитание ответственного отношения к коллективной деятельности.
Целевая аудитория: для 8 класса
Данная разработка может быть использована при изучении окислительно-восстановительных реакций в 11 классе. Содержит описание к лабораторной работе, демонстрирующей наглядный эффект превращения соединений хрома и марганца в различных средах.
Также разработка поможет учителю объяснить учащимся, как изменяются степени окисления хрома и марганца в зависимости от растворяемой среды и какие соединения этих элементов образуются при различных условиях. Разработка содержит задания на закрепление материала.
Разработка содержит задания на закрепление материала.
Разработка урока химии в 8 классе. Задачи данного урока:
систематизировать значение названий и состава сложных веществ;
формировать у учащихся знания о составе оснований, валентности гидроксигруппы, физико-химических свойствах щелочей, их получении;
развивать у учащихся умение сравнивать вещества, выделять общие черты в составе и свойствах оснований.
Цели урока:
развитие умений характеризовать состав оснований по формулам и отличать их от других сложных веществ;
проверка правильности составления и записи уравнений химических реакций, в том числе реакций нейтрализации;
Формирование навыков аккуратной работы с химическими веществами в соответствии с правилами техники безопасности. Данный урок создан по методическим материалам автора Минченкова Е.Е.
Целевая аудитория: учителя
Настоящая разработка урока на тему «Периодический закон и периодическая система химических элементов Д. И. Менделеева в свете теории строения атома» составлена для УМК Гара Н.Н., учебник Химия-11 (Рудзитис Г.Е.) Урок рассчитан на учащихся 11 класса Методическая разработка включает конспект урока химии в 11 классе + презентация
И. Менделеева в свете теории строения атома» составлена для УМК Гара Н.Н., учебник Химия-11 (Рудзитис Г.Е.) Урок рассчитан на учащихся 11 класса Методическая разработка включает конспект урока химии в 11 классе + презентация
Презентация включает иллюстрированный теоретический материал и контрольно-измерительный материал для контроля знаний и умений
Конспект урока химии в 10 классе по ТМЦ Габриелян О.С. с презентацией с активными ссылками на видеоматериалы.
Цели занятия:
- изучить химические свойства одноосновных карбоновых кислот на примере уксусной кислоты;
- вспомнить взаимовлияние атомов в молекулах карбоновых кислот, номенклатура;
- развивать логическое мышление умение обобщать и делать выводы; повторить основные правила безопасности; развивать навыки обращения с лабораторным оборудованием;
- воспитывать культуру речи, умение слушать и правильно излагать свои мысли.
Целевая аудитория: для 10 класса
Мысленный эксперимент, как одно из самых необычных заданий на итоговой аттестации учащихся, вызывает значительные трудности в реализации. Условия работы часто включают описание конкретного химического явления, сопровождаемого определенными характеристиками. Для наиболее полного выполнения заданий данного типа от учащихся требуется знание химических свойств веществ, их названий, то есть понимание любой химической терминологии и умение выражать происходящие процессы в виде записи реакции уравнения. Преподавателю важно в ходе подготовки к этой форме экзамена суметь подвести учащихся к пониманию ключевых слов в описании эксперимента. Данный методический материал посвящен подготовке к выполнению заданий данного типа.
Условия работы часто включают описание конкретного химического явления, сопровождаемого определенными характеристиками. Для наиболее полного выполнения заданий данного типа от учащихся требуется знание химических свойств веществ, их названий, то есть понимание любой химической терминологии и умение выражать происходящие процессы в виде записи реакции уравнения. Преподавателю важно в ходе подготовки к этой форме экзамена суметь подвести учащихся к пониманию ключевых слов в описании эксперимента. Данный методический материал посвящен подготовке к выполнению заданий данного типа.
Целевая аудитория: для 11 класса
Методическая разработка урока по теме «Кислота» включает презентацию и конспект урока. Урок изучения нового материала по теме знакомит учащихся с классом неорганических соединений — кислот, их общей формулой, классификацией, распространением в природе. Также у студентов будет возможность познакомиться с основными неорганическими кислотами.
- 1.
 Первый урок химии 8 класс Люблю химию с первого урока… Химия — непростая наука, ведь не зря ее начинают изучать только в 8 классе, когда у школьников уже есть определенные знания по математике, физике, биологии, географии и др. Но сердца школьников успели покорить и другие предметы и их учителя. Поэтому учитель химии находится в ситуации, когда нужно влюбить учеников в свою науку с первого взгляда, с первого урока. Предлагаю разработку первого урока химии в 8 классе. Этот урок должен показать учащимся, что химия – наука интересная, увлекательная, но в то же время требующая серьезного отношения, большого усердия. На занятиях использую различные формы работы с учащимися: беседа, викторина, игра, лабораторные опыты, демонстрационный эксперимент, рассказ, просмотр видео. Урок сопровождается компьютерной презентацией, демонстрацией видеофрагментов из истории науки, инсценировками в исполнении членов химической секции НОУ (научного объединения студентов). Во время урока необходимо вовлечь в занятие как можно больше учащихся, дать им возможность что-то ответить, выполнить задание или опыт — проявить себя.
Первый урок химии 8 класс Люблю химию с первого урока… Химия — непростая наука, ведь не зря ее начинают изучать только в 8 классе, когда у школьников уже есть определенные знания по математике, физике, биологии, географии и др. Но сердца школьников успели покорить и другие предметы и их учителя. Поэтому учитель химии находится в ситуации, когда нужно влюбить учеников в свою науку с первого взгляда, с первого урока. Предлагаю разработку первого урока химии в 8 классе. Этот урок должен показать учащимся, что химия – наука интересная, увлекательная, но в то же время требующая серьезного отношения, большого усердия. На занятиях использую различные формы работы с учащимися: беседа, викторина, игра, лабораторные опыты, демонстрационный эксперимент, рассказ, просмотр видео. Урок сопровождается компьютерной презентацией, демонстрацией видеофрагментов из истории науки, инсценировками в исполнении членов химической секции НОУ (научного объединения студентов). Во время урока необходимо вовлечь в занятие как можно больше учащихся, дать им возможность что-то ответить, выполнить задание или опыт — проявить себя. Восьмиклассникам свойственно восприятие материала через образы, через собственные впечатления от самостоятельной деятельности, что важно использовать для развития устойчивого интереса к предмету. Чем больше каналов восприятия предлагаемого материала будет использовано, тем больше информации будет усвоено, а эффективность обучения повысится. Поэтому уже на первом занятии учащиеся должны обратить внимание на то, что развитие умений наблюдать, слушать, говорить, думать, анализировать, делать выводы и т. д. будет способствовать лучшему усвоению материала. проводить уроки-праздники в разных классах. Самое удобное время для этого – последний урок четверти или полугодия. Учителем должна быть разработана целая система мероприятий, способствующих развитию познавательного интереса к предмету: первый и последний уроки в учебном году, неделя химии, внеклассные мероприятия, экскурсии, НОУ, участие в конференциях, конкурсах, олимпиадах, и т.д. Задачи урока. Образовательная: познакомить учащихся с предметом химии; дать представление о химии как о точной науке, не лишенной лирики; представить точки зрения на происхождение слова «химия»; показать связь химии с другими науками.
Восьмиклассникам свойственно восприятие материала через образы, через собственные впечатления от самостоятельной деятельности, что важно использовать для развития устойчивого интереса к предмету. Чем больше каналов восприятия предлагаемого материала будет использовано, тем больше информации будет усвоено, а эффективность обучения повысится. Поэтому уже на первом занятии учащиеся должны обратить внимание на то, что развитие умений наблюдать, слушать, говорить, думать, анализировать, делать выводы и т. д. будет способствовать лучшему усвоению материала. проводить уроки-праздники в разных классах. Самое удобное время для этого – последний урок четверти или полугодия. Учителем должна быть разработана целая система мероприятий, способствующих развитию познавательного интереса к предмету: первый и последний уроки в учебном году, неделя химии, внеклассные мероприятия, экскурсии, НОУ, участие в конференциях, конкурсах, олимпиадах, и т.д. Задачи урока. Образовательная: познакомить учащихся с предметом химии; дать представление о химии как о точной науке, не лишенной лирики; представить точки зрения на происхождение слова «химия»; показать связь химии с другими науками. Развивающие: развитие познавательного интереса к предмету; знакомство учащихся с достижениями современной науки, с биографиями великих химиков. Воспитательная: воспитание любви к своему Отечеству, гордости за достижения и успехи нашей страны в области науки; воспитание бережного отношения к своему здоровью; воспитание уважительного отношения к различным точкам зрения других людей. Оборудование и реагенты. Компьютер, видеофрагменты из коллекции модулей ОМС, карточки с вопросами викторины и описаниями веществ, портреты Ж.Ю. Берцелиус, Д.И. Менделеев, Р. Бунзен, Ф.А. Вуд, Н.Н. Зинина; штативы с пробирками, химические стаканчики, тигельные щипцы, спиртовка, фарфоровый стаканчик, коническая колба, щепка; вода, раствор аммиака, раствор уксусной кислоты, спирт этиловый, бензин, соль, сахар, крахмал, мука, кусочки льда, вата, песок речной, опилки, парафин, медный купорос, железные опилки, медная стружка, красный фосфор, сера, растворы KI, Pb(NO3)2, KOH, CuSO4, NaOH, FeCl3, Na2SO4, BaCl2, HCl, Na2CO3, CaCl2, лакмуса, фенолфталеина, дихромата аммония.
Развивающие: развитие познавательного интереса к предмету; знакомство учащихся с достижениями современной науки, с биографиями великих химиков. Воспитательная: воспитание любви к своему Отечеству, гордости за достижения и успехи нашей страны в области науки; воспитание бережного отношения к своему здоровью; воспитание уважительного отношения к различным точкам зрения других людей. Оборудование и реагенты. Компьютер, видеофрагменты из коллекции модулей ОМС, карточки с вопросами викторины и описаниями веществ, портреты Ж.Ю. Берцелиус, Д.И. Менделеев, Р. Бунзен, Ф.А. Вуд, Н.Н. Зинина; штативы с пробирками, химические стаканчики, тигельные щипцы, спиртовка, фарфоровый стаканчик, коническая колба, щепка; вода, раствор аммиака, раствор уксусной кислоты, спирт этиловый, бензин, соль, сахар, крахмал, мука, кусочки льда, вата, песок речной, опилки, парафин, медный купорос, железные опилки, медная стружка, красный фосфор, сера, растворы KI, Pb(NO3)2, KOH, CuSO4, NaOH, FeCl3, Na2SO4, BaCl2, HCl, Na2CO3, CaCl2, лакмуса, фенолфталеина, дихромата аммония. Организация времени. Знакомство с классом.2. Актуализация знаний. Учитель. Какие ассоциации у вас вызывает слово «химия»? К какой группе наук относится химия? Вы уже знаете, как переводятся слова: «география», «геометрия», «биология», но как переводится слово «химия»? Ответы студентов.3. Информация. Учитель. Существует несколько точек зрения на происхождение слова «химия». Демонстрируются видеоролики из коллекции модулей ОМС (РПМЦ — программный продукт Минобразования, http://www.shkola.edu.ru). Учитель. Мы рассмотрим фрагмент «История развития химии» (ммлаб.химия.002и.омс), в котором даны варианты перевода слова «химия». а) Хми (египетское) – «черная» земля. Древнее название Египта, где зародилась наука химия. б) Кеме (египетское) – «черная» наука. Алхимия как темная, дьявольская наука (сравните с колдовством — колдовством, основанным на действии злых духов). в) Хюма (др.-греч.) – «литье» из металлов; того же корня и греческого humos — «сок». г) Ким (древнекитайский) – «золото». Тогда химию можно интерпретировать как «изготовление золота».
Организация времени. Знакомство с классом.2. Актуализация знаний. Учитель. Какие ассоциации у вас вызывает слово «химия»? К какой группе наук относится химия? Вы уже знаете, как переводятся слова: «география», «геометрия», «биология», но как переводится слово «химия»? Ответы студентов.3. Информация. Учитель. Существует несколько точек зрения на происхождение слова «химия». Демонстрируются видеоролики из коллекции модулей ОМС (РПМЦ — программный продукт Минобразования, http://www.shkola.edu.ru). Учитель. Мы рассмотрим фрагмент «История развития химии» (ммлаб.химия.002и.омс), в котором даны варианты перевода слова «химия». а) Хми (египетское) – «черная» земля. Древнее название Египта, где зародилась наука химия. б) Кеме (египетское) – «черная» наука. Алхимия как темная, дьявольская наука (сравните с колдовством — колдовством, основанным на действии злых духов). в) Хюма (др.-греч.) – «литье» из металлов; того же корня и греческого humos — «сок». г) Ким (древнекитайский) – «золото». Тогда химию можно интерпретировать как «изготовление золота».
- 2. 4. Разминка. Учитель. Хотя химия сложная наука, вы уже многое знаете из других наук, из жизненного опыта. Сами увидим: вам предлагаются карточки с вопросами из различных тем курса химии 8, 9, 10 классов. Кто хочет ответить? Вопросы викторины «Так ли сложна химия?» Почему мы дуем на спичку, когда хотим ее потушить? (Выдыхаемый воздух содержит CO2.) Почему горящий бензин нельзя потушить водой? (Бензин легче воды и не смешивается с ней.) Как носить 1 литр воды на ладони, не пролив ни капли? (Замерзает во льду.) Что теплее: три рубашки или тройная рубашка? (Три рубашки.) В каком море не утонешь? Почему? (В Мертвом море очень соленое.) Что тяжелее: 1 кг железа или 1 кг ваты? (Они равны.) Из 1 г какого металла можно вытянуть проволоку длиной 2,5 км? (Из золота.) Можно ли заполнить воздухом только половину воздушного шара? (Это невозможно.) Что означает выражение «как с гуся вода»? (Перья водоплавающих птиц не смачиваются водой.) Соединения каких металлов придают планете Марс красный оттенок? (Соединения железа.
 ) Три одинаковые горящие свечи были одновременно накрыты тремя банками емкостью 0,4 л, 0,6 л и 1 л. Что произойдет в этом случае? (Свеча погаснет тем раньше, чем меньше объем баночки.) После каждого ответа учитель говорит, к какой теме и классу относится вопрос. За правильный ответ учащийся получает на память таблицу растворимости или периодическую таблицу малых размеров. Не все вопросы можно использовать, в зависимости от времени ответов на них, но необходимо сообщить детям, что их новые знания будут основываться на том, что они уже имеют, получили на других уроках, а с трудными вопросами поможет учитель. понять.5. Игра «Угадай вещество». Учитель. Что такое химия без экспериментов? Конечно, вы сами хотите «хим»! Вы знаете подсказки? Вы можете отличить их друг от друга? Проверим… На столе у учителя стоят три лотка с веществами — в одном только бесцветные прозрачные жидкости, в другом только белые твердые вещества, а в третьем — разноцветные твердые вещества. Вещества 1-й лоток. В маленьких стаканчиках: вода, раствор аммиака, раствор уксусной кислоты, спирт этиловый, бензин.
) Три одинаковые горящие свечи были одновременно накрыты тремя банками емкостью 0,4 л, 0,6 л и 1 л. Что произойдет в этом случае? (Свеча погаснет тем раньше, чем меньше объем баночки.) После каждого ответа учитель говорит, к какой теме и классу относится вопрос. За правильный ответ учащийся получает на память таблицу растворимости или периодическую таблицу малых размеров. Не все вопросы можно использовать, в зависимости от времени ответов на них, но необходимо сообщить детям, что их новые знания будут основываться на том, что они уже имеют, получили на других уроках, а с трудными вопросами поможет учитель. понять.5. Игра «Угадай вещество». Учитель. Что такое химия без экспериментов? Конечно, вы сами хотите «хим»! Вы знаете подсказки? Вы можете отличить их друг от друга? Проверим… На столе у учителя стоят три лотка с веществами — в одном только бесцветные прозрачные жидкости, в другом только белые твердые вещества, а в третьем — разноцветные твердые вещества. Вещества 1-й лоток. В маленьких стаканчиках: вода, раствор аммиака, раствор уксусной кислоты, спирт этиловый, бензин. 2-й лоток. В маленьких стаканчиках белые твердые вещества: поваренная соль, сахар, крахмал, мука, кубики льда, вата. 3-й лоток. В чашечках твердые разноцветные вещества: речной песок, опилки, парафин, медный купорос, железные опилки, медная стружка, красный фосфор, сера. Учитель. Нужны трое добровольцев в качестве экспериментаторов, которые попытаются идентифицировать предложенные вещества, обязательно объясняя свои действия. Учитель предупреждает учащихся о соблюдении техники безопасности при выполнении эксперимента. Учащиеся пытаются определить вещества. Показан видеофрагмент — модуль «Алхимическая лаборатория» (ммлаб.химия.омс), дающий представление о жизни и деятельности алхимиков.6. Информация. Интересные факты из жизни ученых-химиков. Разыгрываются заранее подготовленные студентами-членами НОУ инсценировки. Показаны портреты ученых. Повар Берцелиуса. — Не могу точно сказать, — ответила она, — он берет большую фляжку с какой-то жидкостью, наливает ее в маленькую, встряхивает, наливает в еще меньшую, снова встряхивает и наливает в очень маленькую.
2-й лоток. В маленьких стаканчиках белые твердые вещества: поваренная соль, сахар, крахмал, мука, кубики льда, вата. 3-й лоток. В чашечках твердые разноцветные вещества: речной песок, опилки, парафин, медный купорос, железные опилки, медная стружка, красный фосфор, сера. Учитель. Нужны трое добровольцев в качестве экспериментаторов, которые попытаются идентифицировать предложенные вещества, обязательно объясняя свои действия. Учитель предупреждает учащихся о соблюдении техники безопасности при выполнении эксперимента. Учащиеся пытаются определить вещества. Показан видеофрагмент — модуль «Алхимическая лаборатория» (ммлаб.химия.омс), дающий представление о жизни и деятельности алхимиков.6. Информация. Интересные факты из жизни ученых-химиков. Разыгрываются заранее подготовленные студентами-членами НОУ инсценировки. Показаны портреты ученых. Повар Берцелиуса. — Не могу точно сказать, — ответила она, — он берет большую фляжку с какой-то жидкостью, наливает ее в маленькую, встряхивает, наливает в еще меньшую, снова встряхивает и наливает в очень маленькую. один… — А потом? — А потом он все выливает!
один… — А потом? — А потом он все выливает! - 3. Рассказ сопровождается демонстрацией опыта учителем. Для опыта берут 4 колбы разного объема. В большую колбу сначала наливают бесцветный раствор щелочи, колбу меньшего размера предварительно смачивают раствором фенолфталеина. В колбу со сфенолфталеином наливают раствор щелочи, раствор окрашивается в малиновый цвет. В третью колбу, еще меньшую, наливают немного раствора соляной кислоты большей концентрации, чем раствор щелочи, а затем в нее наливают окрашенный раствор щелочи. В третьей колбе раствор обесцвечивается. А когда всю смесь переливают в очень маленькую колбу, в которой находится немного концентрированного раствора щелочи, раствор снова становится малиновым. Покупки для этих работ он обычно делал в Гостиных (1834-1819 гг.).07) двор. Однажды, выбирая нужный товар, он услышал за спиной: «Кто этот почтенный господин?» — Таких людей надо знать, — с уважением в голосе ответил приказчик. — Это Менделеев, чемоданчик! Воры в библиотеке.
 Однажды в кабинет академика Н.Н. Бекетов: «Николай Николаевич! Ученый, не сразу оторвавшись от своих расчетов, спокойно спросил: «Что они там читают?» Сванте Аррениус. Сванте Аррениус очень рано начал набирать вес. Он рассказал историю, связанную со своим лишним весом. Однажды ученые собрались в центральной гостинице Берлина для очередных дебатов. Аррениус оставил пальто в гардеробе и открыл дверь, чтобы присоединиться к коллегам, но гардеробщик остановил его словами: «Вы идете не туда, сударь, рядом сидит мясная корпорация!»7. Чудеса своими руками. На столах учащихся стоят штативы с двумя пробирками. Учитель. Вы сами прекрасные экспериментаторы, с помощью нехитрых трюков можете творить чудеса. Ваша задача смешать содержимое пробирок между собой. Учитель объясняет учащимся правила техники безопасности при выполнении эксперимента. Учитель. Растворы подбираются таким образом, чтобы в каждом случае либо выпадали осадки разного цвета, либо выделялся газ, либо изменялась окраска. Учащиеся проводят эксперимент, наблюдают за происходящими изменениями.
Однажды в кабинет академика Н.Н. Бекетов: «Николай Николаевич! Ученый, не сразу оторвавшись от своих расчетов, спокойно спросил: «Что они там читают?» Сванте Аррениус. Сванте Аррениус очень рано начал набирать вес. Он рассказал историю, связанную со своим лишним весом. Однажды ученые собрались в центральной гостинице Берлина для очередных дебатов. Аррениус оставил пальто в гардеробе и открыл дверь, чтобы присоединиться к коллегам, но гардеробщик остановил его словами: «Вы идете не туда, сударь, рядом сидит мясная корпорация!»7. Чудеса своими руками. На столах учащихся стоят штативы с двумя пробирками. Учитель. Вы сами прекрасные экспериментаторы, с помощью нехитрых трюков можете творить чудеса. Ваша задача смешать содержимое пробирок между собой. Учитель объясняет учащимся правила техники безопасности при выполнении эксперимента. Учитель. Растворы подбираются таким образом, чтобы в каждом случае либо выпадали осадки разного цвета, либо выделялся газ, либо изменялась окраска. Учащиеся проводят эксперимент, наблюдают за происходящими изменениями. (Например, берут растворы йодистого калия и азотнокислого свинца (II); гидроксид калия и сульфат меди (II); гидроксид натрия и хлорид железа (III); сульфат натрия и хлорид бария; лакмус и соляную кислоту, лакмус и гидроксид натрия. , уксусная кислота и карбонат натрия и т. д.) восемь. Поиграем… Игра «Что в черном ящике?» Класс делится на команды по 4 человека. Учитель. Задание на команды: по описанию особенностей свойств, истории открытия, знакомым областям применения нужно угадать, о каком веществе идет речь. Если угадаешь вещество с первой попытки, получишь 5 баллов, со второй — 4 балла и так далее. Ответы даются в письменном виде, чтобы другие команды могли продолжить игру. Если команда дала неверный ответ, она имеет право продолжить игру, но получает минус 1 очко. По результатам двух-трех туров определяется команда-победитель, которая получает приз. Ведущий дает правильный ответ в конце каждого раунда. Баллы сохраняются на доске (можно выбрать помощника из ребят в классе). Первая субстанция1) Эту субстанцию в старину называли владычицей жизни и смерти.
(Например, берут растворы йодистого калия и азотнокислого свинца (II); гидроксид калия и сульфат меди (II); гидроксид натрия и хлорид железа (III); сульфат натрия и хлорид бария; лакмус и соляную кислоту, лакмус и гидроксид натрия. , уксусная кислота и карбонат натрия и т. д.) восемь. Поиграем… Игра «Что в черном ящике?» Класс делится на команды по 4 человека. Учитель. Задание на команды: по описанию особенностей свойств, истории открытия, знакомым областям применения нужно угадать, о каком веществе идет речь. Если угадаешь вещество с первой попытки, получишь 5 баллов, со второй — 4 балла и так далее. Ответы даются в письменном виде, чтобы другие команды могли продолжить игру. Если команда дала неверный ответ, она имеет право продолжить игру, но получает минус 1 очко. По результатам двух-трех туров определяется команда-победитель, которая получает приз. Ведущий дает правильный ответ в конце каждого раунда. Баллы сохраняются на доске (можно выбрать помощника из ребят в классе). Первая субстанция1) Эту субстанцию в старину называли владычицей жизни и смерти. Его приносили в жертву богам, а иногда и поклонялись как божеству. (5 баллов.) 2) Служил мерилом богатства, могущества, выносливости, могущества, считался хранителем молодости и красоты. (4 балла.) 3) По народным поверьям обладает способностью помогать человеку во всех его делах, уберегать его от бед и несчастий. (3 балла.) 4) «Он родится из воды, но воды боится». (2 балла.) 5) Широко используется в быту, в кулинарии, в кожевенном деле, в текстильной промышленности и др. (1 балл) (Ответ. Поваренная соль.) Второе вещество1) Древние египтяне называли его «вааэперэ», что означает «рожденный на небе». (5 баллов.) 2) Древние копты называли его «камнем неба». (4 балла.)
Его приносили в жертву богам, а иногда и поклонялись как божеству. (5 баллов.) 2) Служил мерилом богатства, могущества, выносливости, могущества, считался хранителем молодости и красоты. (4 балла.) 3) По народным поверьям обладает способностью помогать человеку во всех его делах, уберегать его от бед и несчастий. (3 балла.) 4) «Он родится из воды, но воды боится». (2 балла.) 5) Широко используется в быту, в кулинарии, в кожевенном деле, в текстильной промышленности и др. (1 балл) (Ответ. Поваренная соль.) Второе вещество1) Древние египтяне называли его «вааэперэ», что означает «рожденный на небе». (5 баллов.) 2) Древние копты называли его «камнем неба». (4 балла.) - 4. 3) Изделия из него ценились дороже золота. Кольца и броши из него могли делать только очень богатые люди. (3 балла.) 4) Алхимики считали его настолько неблагородным металлом, что с ним не стоило иметь дело. (2 балла.) 5) Его именем назван век. Это пластичный мягкий металл. (1 балл) (Ответ. Железо.) 9. «Знаете ли вы, что…» Мастер.
 Сейчас мы узнаем о достижениях современной науки, об интересных открытиях в области химии и смежных наук. Информация сопровождается компьютерной презентацией, слайды которой иллюстрированы фотографиями, видеороликами, флеш-анимациями и т. д. Нанотехнологии: сегодня и завтра. Нано (от греческого nanos — карлик) — миллиардная часть чего-либо. Область науки, изучающая свойства объектов 10–9м по размеру. Нанотехнологии манипулируют отдельными частицами размером от 1 до 100 нм, а также разрабатывают устройства подобных размеров. Сейчас созданы порошки и суспензии, улучшающие работу двигателей и механизмов. Покрытия из материалов, изготовленных с использованием нанотехнологий, предотвращают появление ржавчины, помогают материалу самоочищаться или не смачиваться водой. Первые нанороботы способны путешествовать по телам животных. Водород можно безопасно хранить с помощью нанотрубок. В будущем можно конструировать любые молекулы и создавать сверхпрочные материалы. В медицине планируется создать лекарство направленного действия, проникающее в пораженную ткань или опухоль; использование нанороботов для диагностики и лечения практически всех заболеваний, выращивание тканей и органов.
Сейчас мы узнаем о достижениях современной науки, об интересных открытиях в области химии и смежных наук. Информация сопровождается компьютерной презентацией, слайды которой иллюстрированы фотографиями, видеороликами, флеш-анимациями и т. д. Нанотехнологии: сегодня и завтра. Нано (от греческого nanos — карлик) — миллиардная часть чего-либо. Область науки, изучающая свойства объектов 10–9м по размеру. Нанотехнологии манипулируют отдельными частицами размером от 1 до 100 нм, а также разрабатывают устройства подобных размеров. Сейчас созданы порошки и суспензии, улучшающие работу двигателей и механизмов. Покрытия из материалов, изготовленных с использованием нанотехнологий, предотвращают появление ржавчины, помогают материалу самоочищаться или не смачиваться водой. Первые нанороботы способны путешествовать по телам животных. Водород можно безопасно хранить с помощью нанотрубок. В будущем можно конструировать любые молекулы и создавать сверхпрочные материалы. В медицине планируется создать лекарство направленного действия, проникающее в пораженную ткань или опухоль; использование нанороботов для диагностики и лечения практически всех заболеваний, выращивание тканей и органов. В электронике это создание сверхминиатюрных электронных устройств, гибких дисплеев, электронной бумаги, новых типов двигателей и топливных элементов (http://www.aif.ru). Многие гляциологи считают, что толщина полярных ледяных щитов сокращается неудержимыми темпами. За 5 лет объем льда, сходящего в Атлантику ежегодно, увеличился почти в 2 раза, что эквивалентно подъему уровня Мирового океана на 0,5 мм в год. Антарктида в период с 2002 по 2005 год ежегодно теряла в среднем 152 км3 льда. К 2100 г. уровень океана может подняться на 4–6 м от современного уровня. Греческие и латинские надписи, сделанные на камнях 2000 лет назад, не читаются из-за разрушившей их эрозии. Для восстановления надписей ученые использовали флуоресцентный метод: при бомбардировке поверхности рентгеновскими лучами атомы приходят в возбужденное состояние, а затем, возвращаясь в состояние покоя, излучают видимый свет. Это позволяет определить следы свинца или железа, оставленные резцом античного автора. Российские химики придумали, как перерабатывать пластиковые бутылки, и синтезировали новый наполнитель для каучуков и полимеров.
В электронике это создание сверхминиатюрных электронных устройств, гибких дисплеев, электронной бумаги, новых типов двигателей и топливных элементов (http://www.aif.ru). Многие гляциологи считают, что толщина полярных ледяных щитов сокращается неудержимыми темпами. За 5 лет объем льда, сходящего в Атлантику ежегодно, увеличился почти в 2 раза, что эквивалентно подъему уровня Мирового океана на 0,5 мм в год. Антарктида в период с 2002 по 2005 год ежегодно теряла в среднем 152 км3 льда. К 2100 г. уровень океана может подняться на 4–6 м от современного уровня. Греческие и латинские надписи, сделанные на камнях 2000 лет назад, не читаются из-за разрушившей их эрозии. Для восстановления надписей ученые использовали флуоресцентный метод: при бомбардировке поверхности рентгеновскими лучами атомы приходят в возбужденное состояние, а затем, возвращаясь в состояние покоя, излучают видимый свет. Это позволяет определить следы свинца или железа, оставленные резцом античного автора. Российские химики придумали, как перерабатывать пластиковые бутылки, и синтезировали новый наполнитель для каучуков и полимеров. Водородное топливо вместо выхлопных газов даст чистую воду. В США разработано прозрачное полимерное покрытие для стен, к которому ничего не прилипает. Это разновидность тефлона. На таком покрытии невозможно писать или рисовать красками, мелом или фломастером. Покрытие может быть использовано для защиты днищ морских судов от обрастания и фюзеляжей самолетов от обледенения.10. Занимательные демонстрационные эксперименты. Учитель. Сегодня было ваше первое знакомство с химией. Конечно, вас ждет что-то необычное, чудесное. Я постараюсь превратиться в волшебника и показать вам чудеса химии. Учитель демонстрирует опыты. «Дым без огня». Две чашки смачивают концентрированными растворами нашатырного спирта и соляной кислоты, а затем подносят друг к другу. Они наблюдают дым без огня. «Из одного стакана — газированная вода, малиновый сок и молоко». В три одинаковых химических стакана наливают бесцветные прозрачные растворы соляной кислоты, хлористого кальция и фенолфталеина. Налейте раствор карбоната натрия в фарфоровую кружку.
Водородное топливо вместо выхлопных газов даст чистую воду. В США разработано прозрачное полимерное покрытие для стен, к которому ничего не прилипает. Это разновидность тефлона. На таком покрытии невозможно писать или рисовать красками, мелом или фломастером. Покрытие может быть использовано для защиты днищ морских судов от обрастания и фюзеляжей самолетов от обледенения.10. Занимательные демонстрационные эксперименты. Учитель. Сегодня было ваше первое знакомство с химией. Конечно, вас ждет что-то необычное, чудесное. Я постараюсь превратиться в волшебника и показать вам чудеса химии. Учитель демонстрирует опыты. «Дым без огня». Две чашки смачивают концентрированными растворами нашатырного спирта и соляной кислоты, а затем подносят друг к другу. Они наблюдают дым без огня. «Из одного стакана — газированная вода, малиновый сок и молоко». В три одинаковых химических стакана наливают бесцветные прозрачные растворы соляной кислоты, хлористого кальция и фенолфталеина. Налейте раствор карбоната натрия в фарфоровую кружку. Затем карбонат натрия выливают из кружки по очереди в каждый из трех стаканов. В первом из них быстро выделяется газ («газировка»), во втором появляется белый осадок («молочный»), а в третьем раствор приобретает малиновый цвет из-за изменения цвета индикатора в щелочной раствор («малиновый сок»). «Платок смачивают в воде, а затем в этиловом спирте. С помощью тигельных щипцов его подносят к горящей спиртовке и поджигают. Несмотря на огромное пламя, платок в итоге остается целым, т.к. спирт воспламеняется и сгорает раньше, чем воспламеняется мокрая тряпка. «Вулкан на столе». На горлышко конической колбы помещают фарфоровую чашку. Под колбу кладут большой лист бумаги. В чашку, слегка смоченную спиртом в центре, наливают бихромат аммония. Они поджигают «вулкан» горящей осколком. Реакция протекает бурно, создается впечатление извергающегося вулкана, из кратера которого изливаются раскаленные массы.
Затем карбонат натрия выливают из кружки по очереди в каждый из трех стаканов. В первом из них быстро выделяется газ («газировка»), во втором появляется белый осадок («молочный»), а в третьем раствор приобретает малиновый цвет из-за изменения цвета индикатора в щелочной раствор («малиновый сок»). «Платок смачивают в воде, а затем в этиловом спирте. С помощью тигельных щипцов его подносят к горящей спиртовке и поджигают. Несмотря на огромное пламя, платок в итоге остается целым, т.к. спирт воспламеняется и сгорает раньше, чем воспламеняется мокрая тряпка. «Вулкан на столе». На горлышко конической колбы помещают фарфоровую чашку. Под колбу кладут большой лист бумаги. В чашку, слегка смоченную спиртом в центре, наливают бихромат аммония. Они поджигают «вулкан» горящей осколком. Реакция протекает бурно, создается впечатление извергающегося вулкана, из кратера которого изливаются раскаленные массы.
Разработано учителем МОУ СОШ №1
Тема: Предмет химия. Вещества. Свойства веществ.
Образовательные задания : Дать учащимся первое представление о предмете химии. Повторить понятия «вещество», «чистые вещества» и «смеси» (связь с естествознанием). Учить определять и описывать свойства некоторых веществ.
Учебные задания . Показать роль химии в научно-техническом прогрессе, ознакомить с успехами в области химии и смежных наук: все, что уже создано и будет создано, есть результат деятельности человека, плод его труда, таланта, и интеллект.
Мотивация . Ответ на вопрос: «Зачем мне изучать химию в школе?»
Оборудование.
1.Сборники «Нефть», «Уголь», «Пластмассы»
2. Альбомы «Деревенская химия; химия и жизнь; наука, обгоняющая мечту; это интересно» и другие, демонстрирующие важность химии в жизни.
3. Предметы лабораторного оборудования и предметы быта, позволяющие показывать одни и те же изделия, изготовленные из разных веществ (стаканы из стекла, фарфора, металла, пластмассы и др. ), и различные изделия из одного вещества (стеклянные колбы, воронки , пробирки, пробирки, холодильник и др.).
), и различные изделия из одного вещества (стеклянные колбы, воронки , пробирки, пробирки, холодильник и др.).
4. Вещества для проведения опытов (указаны в тексте).
ВО ВРЕМЯ ЗАНЯТИЙ
Звонком вхожу в класс, представляюсь, понятно. Обращаю внимание студентов на оснащение кабинета химии. В связи с этим я говорю о правилах поведения в ней и о том, что нужно иметь при себе на каждом занятии. Пишу на доске:
https://pandia.ru/text/78/193/images/image002_125.gif»> Ручка Давайте потрудимся!
На следующий урок прошу ребят принести две тонкие тетради в клетке (для практической и контрольной работы).Показываю справочную литературу по химии и советую по возможности приобрести книги для чтения по химии.Показываю учебники, по которым можно изучать химию не только в школе, но и когда подготовка к поступлению в университет и сдача экзамена
После решения организационных вопросов перехожу к основной части урока. Предлагаю подумать: почему химию начинают изучать в 8-м классе?
Ребята отвечают, что «это сложная наука», «требует большого ума», «сначала нужно изучить биологию, физику, а потом химию» и т. д.
д.
Довожу до мысли, что ответ можно дать после понимания основного ЧТО ХИМИЯ ИЗУЧАЕТ , т.е. что является предметом химии?
Я пишу тему урока на доске, а ученики — в общей тетради. Вспомним, что является предметом изучения ботаники, физики и природоведения. Заметим: все изменения, происходящие в природе, являются природными явлениями, например: дождь, падение осенних листьев, журчание ручья, пение скворца и т. д. Химия вместе с биологией и физикой изучает природу и относится к естественным наукам ; она объясняет, что и как происходит в живой и неживой природе.
Возьмите в руки кусок хлеба, «одно из величайших достижений человеческого разума», в словах — этот чудесный продукт, необходимый для продолжения жизни на Земле, вдохните тончайший, ни с чем не сравнимый хлебный аромат. Прекрасно сказал о нем болгарский поэт Ахсан Баянов в поэме «Хлеб»:
С детства навеки запомнил:
Хлеб – земля. Хлеб — это воздух. Хлеб-вода.
В нем живет солнечное светило,
В нем живет душа родных полей,
Нежность моей доброй матери.
В хлебе жизнь, а в хлебе сила.
Хлеб, который сопровождает каждого из нас от первых шагов до последних дней, рождается на поле.
Они бросили семена в плодородную землю. Как и какие процессы происходят в растениях на свету при фотосинтезе из углекислого газа и воды в зернах хлорофилла и как образуются органические вещества Это наука химия. Рисую на доске зеленый лист (или заранее готовлю рисунок цветными мелками) и схематично показываю процесс образования органического вещества в зеленых листьях.
Даю определение науки химия (оно написано на доске):
«Химия – это наука о веществах, их свойствах и превращениях, а также о явлениях, сопровождающих эти превращения»
Затем переходим к вопросу о различии понятий «физическое тело» и «вещество».
Все предметы, которые нас окружают, называются физическими, а то, из чего они состоят, называется химическими веществами. материал) — стекло, и наоборот, показываю очки из разных веществ (материалов).
Обращаюсь к учащимся, чтобы из следующего списка предметов они выписали отдельно названия веществ и названия тел (предметов): сахар, ключ, сода, льдина, книги, пуговицы, капрон, свеча.
Веществ в природе очень много — более 10 миллионов. В процессе так называемых превращений одни вещества способны переходить (превращаться) в другие.
Показываю опыты.
Опыт 1. При съемках, особенно «боевиков», кровь течет рекой. Для получения «кровавого пятна» используют взаимодействие хлорного железа и роданида калия.
Опыт 2. Получение «малинового сиропа»
К разбавленному раствору щелочи добавить бесцветный спиртовой раствор фенолфталеина.
Опыт 3. Природа повела человека (демонстрирую ржавые предметы).
Итак, вещества характеризуются определенными признаками — цветом, запахом и др.
Даем определения свойствам веществ: свойства вещества — это признаки, по которым они отличаются друг от друга или похожи друг на друга.
Работа с учебником (схема 1, стр. 5).
5).
О значении такой, казалось бы, небольшой детали, как кованый гвоздь, он рассказал в шуточном стихотворении:
Не было гвоздя — пропала подкова,
Не было подковы — лошадь захромала.
Конь захромал — полководец убит,
Конница разбита, войско бежит.
Враг наступает на город, не щадя пленных,
Потому что в кузне не было гвоздя!
Одной из задач химии являются вещества, их свойства и применение в народном хозяйстве.
Еще одна задача — добывать различные вещества. (Показываю сборники «Нефть», «Уголь», «Пластмассы, металлы и сплавы».)
Необычайные успехи в прикладной (практической) химии достигнуты за относительно короткое время, отделяющее нас от эпохи. Разгаданы тайны химического процесса, позволившего природе превратить органические вещества в полезные, для нас сегодня нефть и газ.
Свойства синтезированных веществ часто превосходят творения природы. Все они получены благодаря таланту и кропотливому труду химиков нескольких поколений. Эти чудо-материалы незаметно и прочно вошли в нашу повседневную жизнь.
Эти чудо-материалы незаметно и прочно вошли в нашу повседневную жизнь.
В начале 1970-х любознательные и вездесущие геологи обнаружили в глухом уголке бескрайних сибирских лесов семью Лыковых, несколько десятков лет живших вдали от городов и деревень в полной изоляции от цивилизации.
Это староверы. Что больше всего поразило отшельников среди вещей, принесенных геологами? Прозрачная полиэтиленовая пленка. — Стекло, да мятое, — восхищенно сказал седобородый глава семейства.
Теперь химики могут получать вещества с заданными свойствами; морозостойкие и термостойкие, твердые и мягкие, твердые и упругие, гигроскопичные и влагостойкие и др.
Показываю книгу «Мир химии». Обращаю внимание учащихся на написанный на доске эпиграф:
«Химия широко расставляет руки в делах человеческих…..»
Я останавливаюсь на высказываниях выдающихся людей о химии.
Страстно пропагандируемая химия: «Прежде всего и самым тщательным образом изучайте химию. Знаете, это удивительная наука. Ее зоркий глаз (зрение) проникает и в огненную массу Солнца, и во тьму земной коры, и в невидимые частицы твоего сердца, и в тайны строения камня, и в безмолвную жизнь дерева. Она ищет везде и, всюду находя гармонию, упрямо ищет начало жизни…. И найдет, найдет. Изучая тайны строения материи, она создает в стеклянной колбе живую материю» (М. Горький. «Дети Солнца»).
Знаете, это удивительная наука. Ее зоркий глаз (зрение) проникает и в огненную массу Солнца, и во тьму земной коры, и в невидимые частицы твоего сердца, и в тайны строения камня, и в безмолвную жизнь дерева. Она ищет везде и, всюду находя гармонию, упрямо ищет начало жизни…. И найдет, найдет. Изучая тайны строения материи, она создает в стеклянной колбе живую материю» (М. Горький. «Дети Солнца»).
Зелинский 16 января 1941 г. Обращение к молодежи по радио: «Я всю жизнь увлекался химическими науками, и моя страсть ничуть не ослабла, а, наоборот, еще больше углубилась в настоящее время . Химия часто доставляла мне величайшее удовольствие от познания еще неизведанных тайн природы. Уверен, что никто из интересующихся химией не пожалеет, выбрав эту науку своей специальностью. Итак, химия может многое, но не все. И не надо винить химию и химиков в том, что полимеры пока не могут полностью заменить металлы, а синтетические ткани — шерсть, что антибиотики, часто необходимые для спасения человека, могут нанести вред здоровью, что пестициды и удобрения для сохранения и увеличения урожая, упав в воду, уничтожьте рыбу.
Ты должен винить себя. Опасна не химия, а ее незнание. Безмерный, неразумный энтузиазм всегда приносит вред. Не химия, а мы сами виноваты в том, что, заставив ее работать на себя, не подумали о возможных последствиях. И все же химия приносит людям больше радости, чем огорчения.
Химия — не целина, но и не цветущий сад. Как видите, в ней много работы для тех, кто выбрал ее делом своей жизни. Но, входя в ее прекрасный и загадочный мир, не забудьте узнать об ученых, создавших его. Обязательно познакомьтесь с их жизнью, с их достижениями в области химии. Пусть твои учителя будут…
Литература
Габриелян. 8 класс. М.: Дрофа, 1997. Колтун М. Мир химии. Детская литература 1988.
Урок химии в 8 классе
(презентация вводного урока)
Знакомьтесь, химия!
Учитель химии
Загирова Ирина Николаевна
2014 год
Урок №1
(Вводный урок — презентация)
«Химия обладает неотразимой привлекательностью
благодаря огромной, безграничной силе
она дарит тем, кто ее знает».
Тема: «Знакомьтесь, химия!»
Цель:
Развивать познавательный интерес учащихся 8-х классов к предмету химия.
Задачи:
познакомить учащихся с историей развития химии, дать первые представления об этой науке;
актуализировать знания учащихся о веществах, начать формировать представления о свойствах веществ и их превращениях;
развивать аналитические способности учащихся.
Оборудование.
Тематические стенгазеты, карточки с формулами
вещества и химические реакции, химические мензурки,
фляги плоскодонные, кувшин из темного стекла, спички,
сухое топливо, демонстрационный стол, тигель
щипцы, носовой платок, фарфоровый тигель, наборы металлов и пластмасс.
Вещества.
Свежеприготовленные растворы йодида калия и ацетата свинца,
фенолфталеин, сода кальцинированная, натрия гидросульфат,
этанол, таблетки норсульфазола, дихромат аммония.
Во время занятий
I . введение учителей.
В мире есть наука, без которой сегодня невозможно реализовать самые фантастические проекты и сказочные мечты. Это – ХИМИЯ. В ее копилке немало таких чудес, перед которыми бледнеют фантазии лучших сказочников мира: словно Золушка в принцессу, графит она превращает в блестящий алмаз, бумаге придает прочность металла, а металлу дает память. Недаром ее называют волшебницей и чудотворицей: она кормит, поит, одевает, лечит, моет, добывает полезные ископаемые, позволяет подняться в космос и опуститься на дно океана.
Каждый из вас, сам того не подозревая, каждый день проводит химические реакции, даже не выходя из дома: зажигает спички и газ, готовит еду. Да и само человеческое тело- большая химическая фабрика, на которой происходит множество химических реакций.
Сегодня ваше первое знакомство с этой удивительной наукой. А презентацию проведут учащиеся 9-х классов. Вам расскажут об истории развития науки химия, покажут много интересного опыта, а в конце урока, ответив на вопросы викторины, вы сможете приобрести входные билеты на экспресс, который помчит вас по бескрайним просторам планеты Химия — 8.
Вам расскажут об истории развития науки химия, покажут много интересного опыта, а в конце урока, ответив на вопросы викторины, вы сможете приобрести входные билеты на экспресс, который помчит вас по бескрайним просторам планеты Химия — 8.
II. Изучение нового материала. Демонстрация опытов.
Первый ведущий
В 8 классе вы начинаете изучать новый для вас предмет химия — наука о веществах и их превращениях. Все окружающие нас вещества состоят из химических элементов, которых сейчас более 110. Когда вместе атомы различных элементов образуют более двадцати миллионов веществ.
Знать свойства веществ необходимо, чтобы найти их применение. Да, наши далекие предки ценили необычайную твердость кремния и использовали его для изготовления оружия и инструментов. Некоторые вещества вам уже известны: железо, алюминий, вода, мел, сахар, кислород, углекислый газ, пластмассы и другие (демонстрация коллекций металлов, пластмасс). Не только вещества на Земле, но и вся Вселенная состоит из одних и тех же элементов, которые ученые один за другим открывали на нашей планете.
На уроках химии вы узнаете много интересного о химических элементах. И сегодня мы хотим вкратце познакомить вас с историей развития химии.
студенты
Как правило, большинство историков химии выделяют следующие основные этапы ее развития:
1. Доалхимический период: до III в. год нашей эры
В доалхимический период теоретические и практические аспекты знания о материи развивались относительно независимо друг от друга. Происхождение свойств вещества рассматривалось античной натурфилософией, практические операции с веществом были прерогативой кустарной химии.
2. Алхимический период: III — XVII вв.
Алхимический период, в свою очередь, делится на три подпериода — Александрийский (греко-египетский) арабский и европейский алхимия. Алхимический период – это время поиска философского камня, который считался необходимым для осуществления трансмутации металлов. В этот период произошло зарождение экспериментальной химии и накопление запаса знаний о материи; Алхимическая теория, основанная на древних философских представлениях об элементах, была тесно связана с астрологией и мистикой. Наряду с химико-техническим «золотоделием» алхимический период отличается и созданием своеобразной системы мистической философии.
Наряду с химико-техническим «золотоделием» алхимический период отличается и созданием своеобразной системы мистической философии.
3. Период образования (объединения): XVII — XVIII вв.
В период становления химии как науки произошла ее полная рационализация. Химия освободилась от натурфилософских и алхимических взглядов на элементы как на носителей определенных качеств. Вместе с расширением практических знаний о веществе стали складываться единые взгляды на химические процессы и в полной мере использовать экспериментальный метод. Химическая революция, завершившая этот период, окончательно дала химии вид самостоятельной (хотя и тесно связанной с другими отраслями естествознания) науки, занимающейся экспериментальным изучением состава тел
4. Период количественных законов (атомно-молекулярной теории): 1789 — 1860 гг.
Период количественных законов, отмеченный открытием основных количественных законов химии — стехиометрических законов, и формированием атомно-молекулярной теории, окончательно завершил превращение химии в точную науку, основанную не только на наблюдении, но и также по измерению.
5. Период классической химии: 1860-е — конец XIX в.
Период классической химии характеризуется бурным развитием науки: периодической системы элементов, теории валентности и химического строения молекул, стереохимии, химической термодинамики и химической кинетики; прикладная неорганическая химия и органический синтез. В связи с ростом объема знаний о веществе и его свойствах началась дифференциация химии — выделение ее отдельных разделов, приобретающих черты самостоятельных наук.
6. Современный период: с начала 20 века по настоящее время.
В начале 20 века в физике произошла революция: система знаний о материи, основанная на ньютоновской механике, была заменена квантовой теорией и теорией относительности. Установление делимости атома и создание квантовой механики вложили новое содержание в основные понятия химии. Успехи физики начала 20 в. позволили понять причины периодичности свойств элементов и их соединений, объяснить природу валентных сил, создать теории химической связи между атомами. Появление принципиально новых физических методов исследования предоставило химикам небывалые возможности для изучения состава, строения и реакционной способности веществ. Все это в совокупности привело, в числе прочих достижений, к блестящим успехам биологической химии во второй половине 20 века — установлению строения белков и ДНК, познанию механизмов функционирования клеток живого организма.
Появление принципиально новых физических методов исследования предоставило химикам небывалые возможности для изучения состава, строения и реакционной способности веществ. Все это в совокупности привело, в числе прочих достижений, к блестящим успехам биологической химии во второй половине 20 века — установлению строения белков и ДНК, познанию механизмов функционирования клеток живого организма.
Второй ведущий
Химия зародилась в Египте. Имя» химия » происходит от слова хеми, или хума (черный), которым древние египтяне называли свою страну. Таким образом, слово «химия» означает египетское искусство, которое имело дело с различными минералами и металлами. Химия считалась божественной наукой, находилась в руках жрецов и была скрыта от непосвященных. Арабы добавили к слову «химия» характерную для арабского языка приставку «ал». Появились термины «алхимия» и «алхимик». Сейчас алхимией называют период развития химии с IV по XVI века н.э.
Исследования алхимиков были направлены на поиски «философского камня», якобы способного превратить любой металл в золото. Короли и короли держали в своих дворцах алхимиков, чтобы добывать для них золото. Посмотрите, как работали алхимики.
Короли и короли держали в своих дворцах алхимиков, чтобы добывать для них золото. Посмотрите, как работали алхимики.
Алхимик
— Покажу опыт «Превращение воды в золото».
В одной мензурке находится свежеприготовленный раствор йодистого калия, в другой — раствор ацетата свинца. Оба раствора переливают в мензурку большей вместимости. Выпадает ярко-желтый осадок йодистого свинца (показывает карточку с химической реакцией)
2 КИ + Пб ( Ч 3 СОО ) 2 = ПБИ 2 + 2 КЧ 3 СОО
На последующих уроках мы узнаем, что означают такие записи уравнений химических реакций.
Третий хост
Но алхимикам так и не удалось превратить металлы в золото. Алхимия запрещена во многих странах. Людей, занимавшихся алхимическими исследованиями, обвиняли в колдовстве и сжигали на костре. Но науку нельзя запретить. Ученые отказались от приставки «ал» от слова «алхимия» и получили новое название — химия. так это сейчас называется наука, изучающая окружающие нас вещества, а также их свойства и превращения.
Но науку нельзя запретить. Ученые отказались от приставки «ал» от слова «алхимия» и получили новое название — химия. так это сейчас называется наука, изучающая окружающие нас вещества, а также их свойства и превращения.
На сегодняшний день продукция химического производства занимает главенствующее положение в нашей повседневной жизни. Химические исследования проводятся в лабораториях научно-исследовательских институтов, на заводах, фабриках и т. д. В каждой школе есть кабинет химии и химическая лаборатория.
Теперь познакомимся с некоторыми веществами и химическими превращениями.
Первый лаборант
— Я покажу вам опыт «Превращение воды в малиновый сироп».
Для эксперимента используются четыре химических стакана и банка из темного стекла. В первом стакане находится фенолфталеин, во втором — карбонат натрия, в четвертом — гидросульфат натрия, а в кувшине — вода. В третьем стакане ничего нет.
В кувшине из темного стекла обычная вода, налейте ее в четыре стакана. Затем слейте воду из стаканов, кроме последнего, обратно в кувшин, оставив последний стакан в качестве контроля. Налейте воду из кувшина обратно в стаканы. Смотрите: раствор стал ярко-малиновым, как сироп! Перелейте «сироп» в кувшин, разбавьте его «водой» из последнего стакана. В последний раз переливаем воду из кувшина в стаканы. Смотрите, «сироп» снова превратился в воду.
Затем слейте воду из стаканов, кроме последнего, обратно в кувшин, оставив последний стакан в качестве контроля. Налейте воду из кувшина обратно в стаканы. Смотрите: раствор стал ярко-малиновым, как сироп! Перелейте «сироп» в кувшин, разбавьте его «водой» из последнего стакана. В последний раз переливаем воду из кувшина в стаканы. Смотрите, «сироп» снова превратился в воду.
Кажется, это чудо! Нет, просто в одном стакане был фенолфталеин, в другом — раствор со щелочной средой. При их смешивании образуется раствор малинового цвета. Помните: фенолфталеин в щелочных растворах всегда малиновый. Для того, чтобы цвет исчез, я добавила немного кислого раствора. Кислота нейтрализовала щелочь, и раствор стал бесцветным.
назовите химические вещества, которые использовались в этом эксперименте.
Второй лаборант
— Многие из вас любят сказки и фантастику. Сейчас вы увидите, как из кокона рождается Чужой или просто Змей Горыныч.
(Звучит музыка, демонстрируется опыт Фараона Змея)
Описание опыта
Измельчите таблетку сухого топлива и положите горкой на подставку. Поместите три таблетки норсульфазола поверх топлива. Подожгите сухое топливо. Используйте металлический стержень, чтобы исправить ползающих «змей». После окончания эксперимента потушите огонь, закрыв пластиковую крышку.
Первый лаборант
— Сейчас возьму платок в руки, сначала намочу родниковой водой и подожгу пламенем спички.
(Демонстрируется опыт «Огнеупорный шарф»)
Опыт Описание
Промойте носовой платок водой, затем слегка отожмите и хорошо смочите в спирте. Возьмите платок за один из его концов щипцами для тигля и, удерживая их в вытянутой руке, поднесите к ткани длинную занозу. Спирт тут же вспыхнет — кажется, платок горит. Но горение прекращается, а платок остается невредимым, так как температура воспламенения мокрой тряпки намного выше, чем у спирта.
С 2 Х 5 О + 3 О 2 = 2 СО 2 + 3 Н 2 О
Назовите вещество, поддерживающее процессы горения и дыхания. Что вы знаете о свойствах этого вещества?
Второй лаборант
— В завершение нашей встречи я покажу эксперимент под названием «Вулкан». Вы, конечно, знаете, какое это грандиозное зрелище — извержение вулкана. В древности вулкан Везувий накрывал город Помпеи.
(Звучит музыка, демонстрируется опыт.)
Опыт Описание
Вставьте тигель или фарфоровую чашку в горлышко конической колбы. Колбу можно обмазать пластилином, придав ей форму горы, а можно сделать модель холма. Поместите большой лист бумаги под колбу или макет, чтобы собрать оксид хрома (III). В тигель налить двухромовокислый аммоний, смочить его спиртом в центре горки. Вулкан воспламеняется горящим осколком. Реакция экзотермическая, протекает быстро, вместе с азотом вылетают горячие частицы оксида хрома (III). Если выключить свет, то создается впечатление извергающегося вулкана, из кратера которого вырываются раскаленные массы (показывает карту с химической реакцией).
Реакция экзотермическая, протекает быстро, вместе с азотом вылетают горячие частицы оксида хрома (III). Если выключить свет, то создается впечатление извергающегося вулкана, из кратера которого вырываются раскаленные массы (показывает карту с химической реакцией).
( НХ 4 ) 2 Кр 2 О 7 = Н 2 + Кр 2 О 3 + 4 Н 2 О
(оксид хрома(III) собрать и сохранить для других экспериментов).
Учитель
Вот несколько интересных химических превращений, которые вы должны были наблюдать сегодня на уроке.
О химической реакции можно судить по ее признакам – изменению окраски веществ, появлению запаха, выпадению осадка, выделению света и тепла, образованию газообразного вещества.
— Какие признаки химических реакций вы можете назвать в продемонстрированных опытах?
III.
 Викторина для учащихся
Викторина для учащихсяУчитель
— Ну что, ребята, химия покорила вас своими чудесами? А теперь еще и попробуйте ответить на вопросы викторины, которые будут для вас как бы входными билетами в удивительный мир субстанций и превращений.
Контрольные вопросы
Самое распространенное вещество на Земле. ( Вода)
Не тонет в воде, не горит в огне, существует только при температуре ниже нуля градусов. (Лед)
Назовите металл, который является жидким при комнатной температуре. ( Меркурий)
Без этого газа в мире
Животные и люди не будут жить.
Дети могут назвать его
Ведь его зовут …. Кислород
5) Живу известный на свете, В тринадцатой квартире. Я мягкая, легкая, податливая, Сверкающая в упаковке. ( Алюминий )
6) Этот газ образуется при разрядах молнии. Находится он в сосновом лесу, где легко дышится.
И совсем не оставляет привкуса в воде, За то хорошо ее дезинфицирует. ( Озон )
( Озон )
Молодцы, на все вопросы ответили правильно.
Какие химические вещества вы можете сейчас назвать?
IV. Подведение итогов урока
Учитель:
Мои помощники доказали вам, что химия интересная наука? Что помогло вам убедиться в этом? Какие эксперименты можно повторить дома, чтобы удивить близких? Но не забывайте о безопасности.
А ведь химия — одна из комплексных наук, входящих в раздел естествознания. Миллионы веществ, а значит, миллионы химических формул, химических реакций, множество законов и закономерностей. И вы должны изучить эти законы, законы химии, законы Вселенной. Любой, кто посвятит себя этой науке, может внести свой вклад в разгадку тайн природы, создание новых веществ и материалов, не существующих в природе.
В течение учебного года, от урока к уроку, мы будем постепенно покорять планету — Химия 8, которую мы можем освоить только с помощью наших знаний.
Желаю успехов на этом нелегком, но интересном пути! Удачи!
В.
 Домашнее задание
Домашнее заданиеПо учебнику: Предисловие. Введение. Глава 1.§1 Предмет химии. Вещества. Превращение веществ.
Подготовить доклады (по выбору) по истории химии: «Химические знания древних народов», «Алхимия», «Ятрохимия», «Практическая химия в древней Руси.
Реакции замещения включают взаимодействие. Химическая реакция
Задания с комментариями и решениями
Пример 20. Реакции замещения включают взаимодействие
1) пропилена и воды
2) пропилена и водорода
3) пропилена и хлора 90 при комнатной температуре ) пропен и хлор при 600°С
Разберем предложенные варианты ответов. В первом случае к пропену добавляют воду с образованием пропанола-2. Во втором случае также происходит реакция присоединения, в результате которой образуется пропан. В третьем случае хлор также присоединяется по двойной связи к молекуле пропилена и образуется 1,2-дихлорпропан
И только в четвертом случае происходит реакция замещения — при такой высокой температуре происходит не присоединение хлора по двойной связи, а радикальное замещение атома водорода в метильной группе на хлор.
Пример 21. Реакция уравнением является учитывает другие классификационные признаки реакции: обратимость и изменение степени окисления. Как известно, окисление сернистого ангидрида является обратимым процессом.
Наличие в уравнении реакции простых веществ, из которых образуется сложное вещество, свидетельствует о том, что это окислительно-восстановительная реакция: и сера, и кислород изменяют степени окисления
Пример 22. Взаимодействие масляной кислоты и метанола относится к реакции
1) нейтрализация
2) этерификация
3) гидрирование
4) гидратация
Реакция нейтрализации – это реакция между кислотой и щелочью, в результате которой образуется соль. А вот название реакции «этерификация» (от англ. «ether» — эфир) — как раз соответствует процессу получения сложного эфира из кислоты и спирта. Напомним также, что гидрирование — это процесс присоединения водорода, а гидратация — это присоединение воды.
Таким образом, правильный ответ 2.
Самостоятельные задания
67. К реакциям обмена относятся
1) дегидрирование спиртов
2) галогенирование алканов
3) реакция щелочных металлов с водой
4) реакция нейтрализации
68. Реакции замещения включают взаимодействие хлора с
2) железом
4) алюминием
5) йодидом калия
69. Из указанных типов химических реакций выбирают два типа реакций, к которым относится взаимодействие этана с хлором.
1) присоединение
2) замещение
3) гомогенное
4) каталитическое
5) обратимое
70. Реакции нейтрализации включают взаимодействие веществ
71. Взаимодействие воды с натрием относится к реакциям
1) замещающий
2) каталитический
3) соединения
4) экзотермический
72. Реакция обратима, уравнение которой:
73. Необратима реакция, уравнение которой:
74. Реакция нейтрализации протекает между
Реакция нейтрализации протекает между
1) гидроксидом кальция и азотной кислотой
1 Задания А19 по химии 1. Взаимодействие оксида натрия с водой относится к реакциям 1) необратимым соединениям 2) обменным, обратимым 3) соединениям обратимым 4) обмен, необратимый Оксид натрия – это основной оксид, бурно реагирующий с водой с образованием гидроксида натрия… 2. Укажите реакцию замещения. 1) 2) 3) 4) Признаки реакции замещения в органической химии следующие: из 2 веществ образуется 2 вещества, углеродный скелет не разрушается, атом или группа атомов замещается другим атомом или группой атомов . Эти признаки мы наблюдаем в реакции 1. Ответ: 1.
2 3. Взаимодействие натрия и воды относится к реакциям 1) эндотермическим, каталитическим 2) экзотермическим, каталитическим 3) эндотермическим, обратимым 4) экзотермическим, необратимым Эта реакция протекает с выделением тепла и газообразного водорода (признак необратимости реакции). 4. Взаимодействие кислорода с оксидом серы (IV) относится к реакциям 1) соединение, эндотермическая 2) соединение, экзотермическая 3) замещение, эндотермическая 4) обмен, экзотермическая 2SO2 + O2 = 2 SO3 — реакция соединения, почти все соединение реакции экзотермические. Ответ: 2.
Ответ: 2.
3 5. Окислительно-восстановительные реакции не включают разложение 1) метана 2) азотной кислоты 3) хлорида аммония 4) нитрата аммония Окислительно-восстановительные реакции не включают разложение хлорида аммония, так как образуются аммиак и хлороводород, степени окисления элементы не меняются. Ответ: Взаимодействие глицерина с высшими карбоновыми кислотами относится к реакциям 1) обмена 2) изомеризации 3) присоединения 4) этерификации Реакция между спиртом и кислотой называется реакцией этерификации, она приводит к образованию сложного эфира.
4 7. Взаимодействие карбоната калия с раствором хлорида магния относится к реакциям 1) разложения 2) обмена 3) замещения 4) соединений Реакция обмена — это реакция, протекающая между двумя сложными веществами, в результате которой они обменивают составные части… 8. При нагревании дихромата аммония происходит реакция 1) обмена 2) замещения 3) разложения 4) соединения Соли аммония термически неустойчивы. При нагревании дихромат аммония разлагается с образованием азота, оксида хрома (III) и воды. Ответ: 3.
Ответ: 3.
5 9. Обменные реакции включают взаимодействие между 1) этиленом и водой 2) соляной кислотой и магнием 3) ацетиленом и бромом 4) уксусной кислотой и гидроксидом магния Реакции обмена происходят между двумя сложными веществами, в результате которых вещества обмениваются своими составляющие. Из списка это реакция между уксусной кислотой и гидроксидом магния 2Сh4COOH + Mg(OH) 2 = (Ch4COO) 2Mg + 2h3O 10. При нагревании нитрата меди(II) протекает реакция 1) замещения 2) обмена 3) соединение 4) разложение нагреванием нитрата меди(II), протекает реакция разложения: 2Cu(NO3) 2 = 2CuO + 4NO2 + O2
6 11. Хлорирование бензола на свету относится к реакции 1) замещения 2) присоединения 3) обмена 4) разложения Примечание — хлорирование на свету, без катализатора. Это образует 1,2,3,4,5,6-гексахлорциклогексан. Реакция добавления. Ответ: Взаимодействие оксида фосфора (v) с водой относится к реакциям 1) соединение, эндотермическая 2) соединение, экзотермическая 3) обменная, экзотермическая 4) замещения, экзотермическая экзотермическая реакция соединения. Ответ: 2.
Ответ: 2.
7 13. Взаимодействие оксида кальция с водой относится к реакциям 1) замещения, экзотермическая 2) соединения, экзотермическая 3) соединения, экзотермическая 4) обменная, экзотермическая Ответ: 3. экзотермическая реакция соединения. 14. Реакция, уравнение которой относится к реакциям 1) окислительно-восстановительная, замещения 2) экзотермическая, обменная 3) эндотермическая, соединения 4) каталитическая, разложение Реакции с участием галогенов и водорода — безусловно, реакция соединения. В данном случае эта реакция является эндотермической.
8 Ответ: Взаимодействие кислорода с оксидом серы (IV) относится к реакциям 1) соединение необратимое 2) соединение обратимое 3) замещение, эндотермическое 4) обменное, экзотермическое Взаимодействие кислорода с оксидом серы (IV ) с образованием оксида серы (VI) относится к одному из важнейших примеров обратимых реакций. 16. При нагревании смеси железа и серы протекает реакция 1) соединения 2) обмена 3) замещения 4) распада При взаимодействии двух простых веществ может протекать только реакция соединения. Ответ: 1.
Ответ: 1.
9 17. Взаимодействие сульфида натрия с соляной кислотой относится к 1) замещению 2) разложению 3) соединениям 4) обмену Это реакция обмена: 18. Взаимодействие водорода с хлором относится к реакциям 1) разложения, эндотермические 2) обменные, экзотермические 3) соединения, эндотермические 4) соединения, экзотермические
10 Взаимодействие водорода с хлором относится к реакциям соединения, экзотермическое 19. Взаимодействие кислорода с литием относится к реакциям 1) соединений , эндотермическая 2) соединения, экзотермическая 3) замещения, эндотермическая 4) обменная, экзотермическая Это реакция соединения, протекающая с большим выделением тепла. 20. Реакция нейтрализации соответствует уравнению: 1) 2) 3) 4)
11 Реакция нейтрализации по определению – это взаимодействие кислоты и щелочи, в этом списке только один такой вариант.
Химическая реакция. Условия и признаки химических реакций. Химические уравнения 1. Какое уравнение соответствует реакции разложения? 2. Какое уравнение соответствует реакции обмена? 3. Что
Какое уравнение соответствует реакции обмена? 3. Что
1. Какое уравнение соответствует реакции разложения? 2. Какое уравнение соответствует реакции обмена? 3. Какое уравнение соответствует реакции замещения? 4. В реакции разложения, сопровождающейся изменением
1. Из предложенного списка веществ выбрать два вещества, с каждым из которых железо реагирует без нагревания. хлорид цинка медь (ii) сульфат кислота азотная концентрированная кислота соляная разбавленная
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ ЛУГАНСКОЙ НАРОДНОЙ РЕСПУБЛИКИ ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ ДОПОЛНИТЕЛЬНОГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ ЛУГАНСКОЙ НАРОДНОЙ РЕСПУБЛИКИ «РЕПУБЛИКАНСКИЙ ЦЕНТР РАЗВИТИЯ ОБРАЗОВАНИЯ» в химия 1. Цинк взаимодействует с раствором Металлы взаимодействуют с растворами солей менее активных металлов. Mg, Na, Ca являются более активными металлами, чем цинк, поэтому реакция с этими солями невозможна.
Вариант 1743654 1. Определите атомы, два из которых из указанных элементов имеют один неспаренный электрон в основном состоянии. 2. Запишите номера выбранных элементов в поле ответа. Выберите три позиции,
2. Запишите номера выбранных элементов в поле ответа. Выберите три позиции,
2 Пояснительная записка Программа разработана на основе обязательного минимума содержания среднего (полного) общего образования по химии. Содержание программы 1. Предмет и задачи по химии. Физические явления
Банк задач 11 класс химия 1. Электронная конфигурация соответствует иону: 2. Частицы и и и и и имеют одинаковую конфигурацию 3. Атомы магния и имеют аналогичную конфигурацию внешнего энергетического уровня .
ЭКЗАМЕНАЦИОННЫЕ БИЛЕТЫ ГОСУДАРСТВЕННОЙ ИТОГОВОЙ АТТЕСТАЦИИ ПО ХИМИИ ПО ОСНОВНЫМ ОБРАЗОВАТЕЛЬНЫМ ПРОГРАММАМ ОСНОВНОГО ОБЩЕГО ОБРАЗОВАНИЯ в 2019 году 1. Периодический закон и периодическая система химических веществ
Задания 5. Простые и сложные вещества. Неорганические вещества 1. Вещества, формулами которых и являются соответственно амфотерный гидроксид и кислота амфотерный гидроксид и соль с основанием и кислотой
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА 8 Конаково «Согласованная» О Школе управления Протокол 2016 года Руководитель Школы управления «Утвержденный» Директор МБОУ СОШ 8 Конаково
Банк заданий по химии 10 класс 1. С каждым из указанных веществ: хлористый водород, водород, бром вода будут реагировать пропан метан этилен 5) ацетилен 2. При выполнении задания из предложенного списка
С каждым из указанных веществ: хлористый водород, водород, бром вода будут реагировать пропан метан этилен 5) ацетилен 2. При выполнении задания из предложенного списка
Задания А12 по химии 1. В схеме превращения Вещества «Х» и «У» соответственно Железо окисляется только до очень сильных окислителей (например, таких как хлор). В реакциях с Сохой: вещество
ЭКЗАМЕНАЦИОННЫЕ БИЛЕТЫ ГОСУДАРСТВЕННОЙ ИТОГОВОЙ АТТЕСТАЦИИ ПО ХИМИИ ДЛЯ ОСНОВНЫХ ОБЩЕОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ в 2018 году БИЛЕТ 1 1. Периодический закон и периодическая система химических элементов Д.И.
A11 Химия Задания 1. Сульфид железа (ii) реагирует с раствором каждого из двух веществ: Сульфид железа (II) является нерастворимой солью, поэтому с другими солями он не будет реагировать, но будет реагировать
Билеты на переводной экзамен по химии в 8 класс Билет 1 1. Предмет химия. Вещества. Вещества бывают простые и сложные. Свойства веществ. 2. Кислоты. Их классификация и свойства. Билет 2 1. Превращения веществ.
Билет 2 1. Превращения веществ.
Муниципальное автономное образовательное учреждение основная общеобразовательная школа д. Зарубино Билеты на химию Учитель химии Сомова Н.Х. 2012 Экзаменационные билеты по химии Теоретическая
Итоговая контрольная по химии 11 класс с ответами >> Итоговая контрольная по химии 11 класс с ответами Итоговая контрольная по химии 11 класс с ответами В лаборатории уксусную кислоту получают по схеме: 1 2 3 4 Ответ: 2 Задание
Скорость реакции, ее зависимость от различных факторов 1. Для увеличения скорости реакции необходимо повысить давление добавить угарный газ (1в) охладить систему удалить угарный газ (1в) 2. Скорость
1. ПЛАНИРУЕМЫЕ РЕЗУЛЬТАТЫ РАЗВИТИЯ ТЕМАТИКИ. В результате изучения предмета в 9 классе учащийся должен знать/понимать: химические символы: знаки химических элементов, формулы химических веществ и уравнения
Задания А25 по химии 1. Серная кислота проявляет окислительные свойства в реакции, схема которой: Окислители забирают электроны и понижают степень окисления. Серная кислота может проявлять окислительное действие
Серная кислота может проявлять окислительное действие
Пояснительная записка Рабочая программа по химии составлена на основании следующих документов: Государственный стандарт общего образования Министерства образования Российской Федерации от 05.03.2004. 1089. Образец программы,
Экзаменационные билеты по химии для государственной (итоговой) аттестации выпускников 9 классов в 2010 2011 учебном году БИЛЕТ 1 1. Периодический закон и периодическая система химических элементов Д.И.Менделеева.
1. Осадок не образуется при взаимодействии водных растворов и и и и 2. Осадок не образуется при взаимодействии водных растворов и и и и 3. Вода образуется в реакции ионного обмена при взаимодействии и и и и
1. ПЛАНИРУЕМЫЕ РЕЗУЛЬТАТЫ ОБУЧЕНИЯ Раздел 2. Многообразие химических реакций В результате изучения раздела учащиеся должны усвоить важнейшие химические понятия: классификация химических реакций различными путями,
Билет 4 1. Виды химической связи: ковалентные (полярные и неполярные), ионные, их сходства и различия. 2. Опыт. Проведение реакций, характерных для кислот (например, соляной кислоты). Билет 5
2. Опыт. Проведение реакций, характерных для кислот (например, соляной кислоты). Билет 5
Тематическое планирование 9 класс/n Содержание Формулировка темы урока Количество часов Повторение основных вопросов 8 класса (3 часа). Периодический закон и химические элементы периодической системы Д.И.
ЭКЗАМЕНАЦИОННАЯ ТЕСТ ПО ХИМИИ (ЭКСТЕРНАТ 9 КЛАСС) 1. Химическая реакция, протекающая с образованием осадка а) h 2 SO 4 + BaCl 2 б) HNO 3 + КОН в) HCl + CO 2 г) HCl + Ag 2 С каким из веществ а) карбонатом
Вариант 5, часть 1 При выполнении заданий этой части в бланке ответов М я под номером выполняемого задания (А1 — А30) ставится «х» в ящик, номер которого соответствует выбранному вами номеру
БИЛЕТЫ ПО ХИМИИ 10-11 КЛАСС. БИЛЕТ 1 1. Периодический закон и периодическая система химических элементов Д.И. Менделеева на основе представлений о строении атомов. Значение периодического закона для
Задания Б7 по химии 1. Фенол реагирует с 1) хлором 2) бутаном 3) серой 4) гидроксидом натрия 5) азотной кислотой 6) оксидом кремния (IV) Фенолы — кислородсодержащие органические соединения в молекула которого
ПРОГРАММА ВСТУПИТЕЛЬНОГО ЭКЗАМЕНА ПО ХИМИИ Абитуриент должен показать знание основных теоретических положений химии как одной из важнейших естественных наук, лежащих в основе научного понимания
Демонстрационная версия промежуточного контроля по химии 2017 2018 уч. г. (профильный класс, учебник Габриелян О.С.). 11 класс (профильный уровень) Вариант 5 Часть1. Ответом на задания 1-20 является последовательность
г. (профильный класс, учебник Габриелян О.С.). 11 класс (профильный уровень) Вариант 5 Часть1. Ответом на задания 1-20 является последовательность
УТВЕРЖДЕНО Приказом Министра образования Республики Беларусь 03.12.2018 836 Билеты на сдачу экзамена экстерном при освоении содержания образовательной программы среднего образования для академических
УТВЕРЖДЕНО Приказом Министра образования Республики Беларусь 03.12.2018 836 Билеты на сдачу экзамена экстерном при освоении содержания образовательной программы основного образования в образовательной
Тест по теме «Химическая связь» 11 класс 1. В аммиаке и хлористом барии химическая связь соответственно 1) ионная и ковалентная полярная 2) ковалентная полярная и ионная 3) ковалентная неполярная и металлическая
8 класс Пояснительная записка Настоящая рабочая программа составлена на основе Типовой программы среднего (полного) общего образования по химии (базовый уровень) для 8 9 классов, рекомендованной письмом
Задания А16 по химии 1. Формальдегид не вступает в реакцию с Формальдегидом является формальдегидом , это тоже метаналь; 40-процентный раствор формальдегида в воде называется формалином. Реакции присоединения идут по карбонильной группе 9.0005
Формальдегид не вступает в реакцию с Формальдегидом является формальдегидом , это тоже метаналь; 40-процентный раствор формальдегида в воде называется формалином. Реакции присоединения идут по карбонильной группе 9.0005
A9 Химия Задания 1. Какой оксид реагирует с раствором, но не реагирует с раствором? MgO Основной оксид, так как Mg является металлом со степенью окисления +2. Основные оксиды реагируют с кислотами кислотные оксиды,
Громченко И.А. Сборник задач по химии для 8 класса МОЦ 109 2009 1. Массовая доля элемента. Расчеты по формулам. 1.1. Какое вещество имеет более тяжелую молекулу: BaO, P 2 O 5, Fe 2 O 3? 1.2.
1. Какой из следующих неметаллов является наиболее типичным? 1) Кислород 2) Сера 3) Селен 4) Теллур 2. Какой из перечисленных элементов имеет наибольшую электроотрицательность? 1) Натрий
Пояснительная записка Изучение химии на уровне основного общего образования направлено на достижение следующих целей: овладение важнейшими знаниями об основных понятиях и законах химии, химической символике;
ХИМИЯ Вариант 0000 Инструкция для поступающих На выполнение экзаменационной работы отводится 3 часа (180 минут). Работа состоит из 2 частей, включающих 40 заданий. Если задание невозможно выполнить сразу,
Работа состоит из 2 частей, включающих 40 заданий. Если задание невозможно выполнить сразу,
Контрольные материалы к элективному курсу «Решение задач повышенной сложности» для 0 класса Номер задания Входной контроль Кодификатор элементов содержания и требований к уровню подготовки выпускников
Планируемые предметные результаты освоения учебного предмета В результате изучения химии обучающийся должен: знать/понимать химические символы: символы химических элементов, формулы веществ и уравнения химических веществ
Требования к уровню подготовки выпускники: В результате изучения химии учащийся должен знать/понимать: химические символы: знаки химических элементов, формулы химических веществ и уравнения химических веществ
Аннотация к рабочей программе по химии 9 класс. 1. Место предмета в структуре основной образовательной программы школы. Рабочая программа по химии для 9 класса реализуется в общеобразовательном классе
ПРИМЕРНОЕ КАЛЕНДАРНОЕ ПЛАНИРОВАНИЕ УЧЕБНОГО МАТЕРИАЛА ХИМИЯ-8 на 2014/2015 учебный год Составлено на основе государственной программы Минченкова Е. Е. по 2 часа в неделю (70 часов в год) Работы I полугодие
Е. по 2 часа в неделю (70 часов в год) Работы I полугодие
ФИПИ Пробное ОГЭ 2018 по химии Вариант обучения 1 Подготовила Мустафина Екатерина Андреевна 1 На рисунке представлена модель атома 1) бора 2) алюминия 3) азота 4) бериллия 2 Радиус атома
Демонстрационный вариант промежуточной аттестации по химии 11 класс 2017-2018 уч.г. 1. Задание Определить, какие атомы двух из указанных в ряду элементов имеют единицу на внешнем энергетическом уровне
Задания А20 по химии 1. Курс реакции азота с водородом уменьшится при 1) понижении температуры 2) повышении концентрации азота 3) использовании катализатора 4) повышении давления Факторы влияющие «за 9учащиеся 5-х классов г. Кежемский 208 Планируемые результаты
Настоящая рабочая программа составлена на основе: Федерального закона от 29 декабря 2012 г. № 273-ФЗ «Об образовании в Российской Федерации»; Порядок организации и осуществления образовательной деятельности по
Муниципальное бюджетное общеобразовательное учреждение, общеобразовательная школа 4 г. Балтийска. Рабочая программа предмета «Химия» 9 класс базовый уровень Балтийск 2017 1.Объяснительная
Балтийска. Рабочая программа предмета «Химия» 9 класс базовый уровень Балтийск 2017 1.Объяснительная
Банк заданий 10 класс часть С (17 заданий). Промежуточная аттестация 2018. 1. Циклопропан + KMnO 4 + H 2 SO 4 = 2. Циклопропан + KMnO 4 + H 2 O = 3. Циклопентен + KMnO 4 + H 2 SO 4 = 4. CH 3 -CH 2 — СН = СН
ЭКЗАМЕНАЦИОННЫЕ БИЛЕТЫ ГОСУДАРСТВЕННОЙ ИТОГОВОЙ АТТЕСТАЦИИ ПО ХИМИИ ДЛЯ ОСНОВНЫХ ОБЩЕОБРАЗОВАТЕЛЬНЫХ ПРОГРАММ Билет 1 1. Периодическая таблица химических элементов Д.И. Менделеева и строение атомов:
Министерство образования и науки Российской Федерации САРАТОВСКИЙ НАЦИОНАЛЬНЫЙ НАУЧНЫЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ИМЕНИ Н. Г. ЧЕРНЫШЕВСКОГО Программа вступительных испытаний в бакалавриат/специальность
Задания для подготовки 1. При сжигании сульфида железа (II) в кислороде выделяется 28 литров диоксида серы (в пересчете на нормальные условия). Рассчитайте массу исходного соединения железа в граммах. Ответ
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА Статус документа Рабочая программа по химии составлена для 9 класса на основании Типовой программы основного общего образования по химии. В рабочей программе определен перечень демонстраций,
В рабочей программе определен перечень демонстраций,
4. Задания на нахождение массы (объема, количества вещества), массовой (объемной) доли продукта реакции и массовой доли (массы) химического соединения в смеси. Решение проблемы нужно начинать с анализа
Банк задач по химии 9 класс 1. Элемент имеет три электрона на 2-м энергетическом уровне. Порядковый номер элемента 3 5 7 13 2. Сколько электронов находится на внешнем уровне элемента с порядковым номером
Требования к уровню подготовки учащихся После изучения материала в 9 классе учащиеся должны: Называть химические элементы по символы, вещества по формулам, знаки и условия осуществления химических реакций,
Описание презентации по отдельным слайдам:
1 слайд
Описание слайда:
2 слайда
Описание слайда:
Задача 1. Реакции замещения включают взаимодействие 1) воды с этиленом 2) воды с ацетиленом 3) хлора с метаном 4) хлора с этеном Задача 2. Взаимодействие глицерина с высшими карбоновыми кислотами относится к реакциям 1) обмена 2) изомеризация 3) присоединение 4) этерификация Задача 3. Взаимодействие хлорида меди (II) с железом относится к реакциям 1) разложения 2) обмена 3) замещения 4) соединения Задача 4. Взаимодействие карбоната калия с раствором хлорида магния относится к реакциям 1) разложения 2) обмена 3) замещения 4) соединения
Взаимодействие глицерина с высшими карбоновыми кислотами относится к реакциям 1) обмена 2) изомеризация 3) присоединение 4) этерификация Задача 3. Взаимодействие хлорида меди (II) с железом относится к реакциям 1) разложения 2) обмена 3) замещения 4) соединения Задача 4. Взаимодействие карбоната калия с раствором хлорида магния относится к реакциям 1) разложения 2) обмена 3) замещения 4) соединения
3 слайда
Описание слайда:
Задача 5. К реакциям гидрирования относится взаимодействие водорода с 1) кислородом 2) фтором 3) ацетиленом 4) оксидом свинца Задача 6. Взаимодействие углерода с кислородом относится к реакциям 1) замещения, экзотермическим 2) соединениям, экзотермическим 3) обменный, эндотермический 4) соединения, эндотермический Задача 7. Реакции замещения включают взаимодействие 1) ацетилена с хлором 2) этилена с хлором 3) бензола с хлором в присутствии катализатора 4) бутадиена-1,3 с хлором Задача 8. Взаимодействие оксида серы (IV) с кислородом относится к реакциям 1) соединения, экзотермические 2) замещения, экзотермические 3) обменные, эндотермические 4) соединения, эндотермические
4 слайда
Описание слайда:
Задача 9. При нагревании бихромата аммония протекает реакция 1) обмена 2) замещения 3) разложения 4) соединения Задача 10. Взаимодействие водорода с кислородом относится к реакциям 1) разложения, эндотермической 2) обменной, экзотермической 3) соединения, эндотермические 4) соединения, экзотермические Задача 11. Обменные реакции включают взаимодействие между 1) этиленом и водой 2) соляной кислотой и магнием 3) ацетиленом и бромом 4) уксусной кислотой и гидроксидом магния Задача 12. При нагревании карбоната аммония образуется происходит реакция 1) соединения 2) обмена 3) замещения 4) разложения
При нагревании бихромата аммония протекает реакция 1) обмена 2) замещения 3) разложения 4) соединения Задача 10. Взаимодействие водорода с кислородом относится к реакциям 1) разложения, эндотермической 2) обменной, экзотермической 3) соединения, эндотермические 4) соединения, экзотермические Задача 11. Обменные реакции включают взаимодействие между 1) этиленом и водой 2) соляной кислотой и магнием 3) ацетиленом и бромом 4) уксусной кислотой и гидроксидом магния Задача 12. При нагревании карбоната аммония образуется происходит реакция 1) соединения 2) обмена 3) замещения 4) разложения
5 слайдов
Описание слайда:
Задача 13. К окислительно-восстановительным реакциям не относятся реакции разложения 1) метана 2) азотной кислоты 3) хлористого аммония 4) аммиачной селитры Задача 14. Взаимодействие водорода с хлором относится к реакциям 1) разложения, эндотермической 2) обменной, экзотермической 3 ) соединения, эндотермические 4) соединения, экзотермические Задача 15.


 Учебник — Габриелян О.С., Остроумов И.Г., Сладков С.А. cкачать в PDF.
Учебник — Габриелян О.С., Остроумов И.Г., Сладков С.А. cкачать в PDF. В. и др.
В. и др. Ко всем заданиям пособия даны подробные ответы с пояснениями.
Ко всем заданиям пособия даны подробные ответы с пояснениями.
 Также приходится изучать химию в 8 классе, которая вызывает большие трудности у школьников. Решением данной проблемы является использование решебников или гдз по химии 8 класс, которые помогут Вам преодолеть страх перед новым учителем и направить на правильный путь изучения химии.
Также приходится изучать химию в 8 классе, которая вызывает большие трудности у школьников. Решением данной проблемы является использование решебников или гдз по химии 8 класс, которые помогут Вам преодолеть страх перед новым учителем и направить на правильный путь изучения химии. Особенно влияет то, что другие предметы тоже требуют большого внимания и на химию времени часто не остаётся.
Особенно влияет то, что другие предметы тоже требуют большого внимания и на химию времени часто не остаётся. ru
ru Перейти к описанию. Поиск в решебнике.
Перейти к описанию. Поиск в решебнике. com
com
 ru
ru
 И. Менделеева, более подробно узнаете о строении атома, ковалентной, ионной и металлической связях, процессах окисления и восстановления, а также о растворах.
И. Менделеева, более подробно узнаете о строении атома, ковалентной, ионной и металлической связях, процессах окисления и восстановления, а также о растворах. Г. Фельдмана 2019. Глава I. Первоначальные химические понятия.
Г. Фельдмана 2019. Глава I. Первоначальные химические понятия. С., являющегося классической основой изучения химии в 8 классах российских средних школ.
С., являющегося классической основой изучения химии в 8 классах российских средних школ. Решебники подойдут как учащимся 8 классов для самоконтроля, так и их родителям для проверки детей.
Решебники подойдут как учащимся 8 классов для самоконтроля, так и их родителям для проверки детей. Н. Гара 8-9 класс
Н. Гара 8-9 класс Е. Рудзитис 8 класс
Е. Рудзитис 8 класс Е. 8 класс
Е. 8 класс С. Гузей 8 класс
С. Гузей 8 класс И. Новошинский Н.С. Новошинская
И. Новошинский Н.С. Новошинская И.
И. Е. Красицкий В.А.
Е. Красицкий В.А. И. Борушко
И. Борушко Е. Шиманович
Е. Шиманович В. Еремина Н.Е. Кузьменко
В. Еремина Н.Е. Кузьменко Н. Ахметов М.А.
Н. Ахметов М.А. Л. 8 класс
Л. 8 класс С. 8 класс
С. 8 класс М. Радецкий
М. Радецкий Л., Ходаков Ю.В., Додонов Ю.Б.
Л., Ходаков Ю.В., Додонов Ю.Б. Е. Кузнецова, А.Н. Левкин
Е. Кузнецова, А.Н. Левкин Н. Гара, Н.И. Габрусева
Н. Гара, Н.И. Габрусева Е., Титова И.М., Гара Н.Н.
Е., Титова И.М., Гара Н.Н. С. Габриелян, А.В. Купцова
С. Габриелян, А.В. Купцова В., Кузьменко Н.Е., Дроздов А.А.
В., Кузьменко Н.Е., Дроздов А.А. Н., Ахметов М.А.
Н., Ахметов М.А. Н.
Н. Л., Бирюлина Е.В., Дмитриева Е.Н.
Л., Бирюлина Е.В., Дмитриева Е.Н. Н., Пашуто Е.Н., Власовец Е.Н.
Н., Пашуто Е.Н., Власовец Е.Н. С., Остроумов И.Г., Сладков С.А.
С., Остроумов И.Г., Сладков С.А. С., Сладков С.А.
С., Сладков С.А. Б., Сакарьянова К.Н., Сахариева Б.Н.
Б., Сакарьянова К.Н., Сахариева Б.Н. А., Корнилаев С.В., Шалашова М.М.
А., Корнилаев С.В., Шалашова М.М. С., Березкин П.Н., Ушакова А.А.
С., Березкин П.Н., Ушакова А.А. А.
А. А. Рябов
А. Рябов А. Боровских
А. Боровских Л., Власовец Е.Н., Гарбар Е.Е., Синявская Т.С.
Л., Власовец Е.Н., Гарбар Е.Е., Синявская Т.С.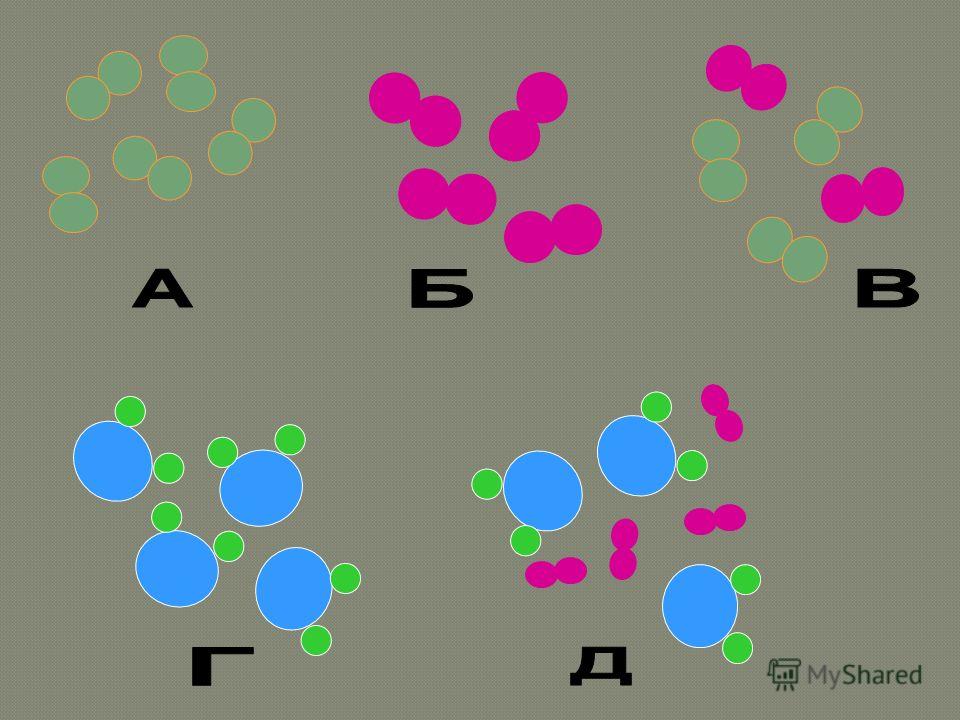 С., Лысова Г.Г.
С., Лысова Г.Г. С. Габриелян, И.В. Аксенова, И.Г. Остроумов
С. Габриелян, И.В. Аксенова, И.Г. Остроумов С. Атанасян, В.Ф. Бутузов, С.Б. Кадомцев, Э.Г. Позняк, И.И. Юдин
С. Атанасян, В.Ф. Бутузов, С.Б. Кадомцев, Э.Г. Позняк, И.И. Юдин П. Дронов, И. И. Баринова, В. Я. Ром, А. А. Лобжанидзе
П. Дронов, И. И. Баринова, В. Я. Ром, А. А. Лобжанидзе В., Родина Н.А., Белага В.В., Ломаченков И.А., Панебратцев Ю.А.
В., Родина Н.А., Белага В.В., Ломаченков И.А., Панебратцев Ю.А. Н., Бунеева Е.В., Комиссарова Л.Ю., Текучева И.В.
Н., Бунеева Е.В., Комиссарова Л.Ю., Текучева И.В.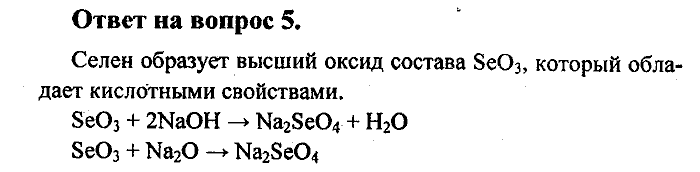 Н. Хвалюк
Н. Хвалюк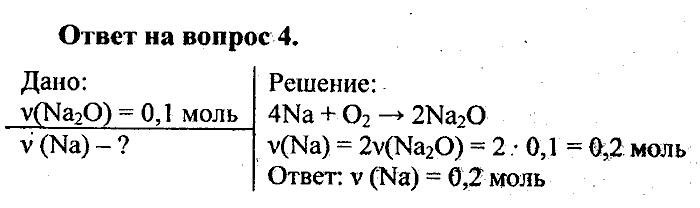 Е.
Е. Е.
Е. М. Радецкий
М. Радецкий А,
А, С.
С. М. Буринськая
М. Буринськая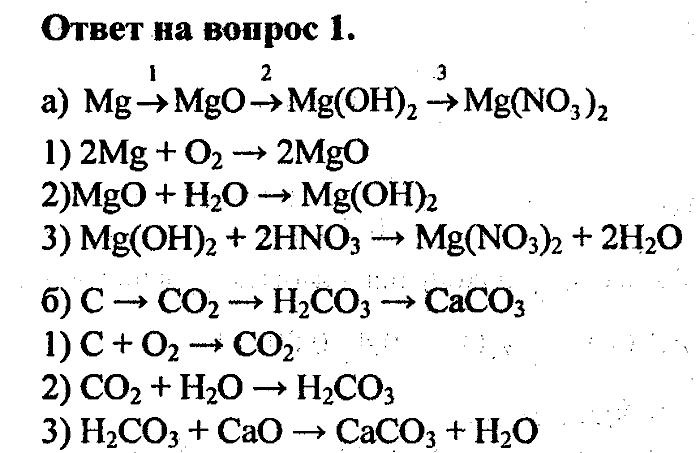 С., Гладюк М.М.
С., Гладюк М.М.