ГДЗ (Ответы) Хімія 8 клас Григорович 2016. Відповіді, решебник к учебнику
ГДЗ Хімія 8 клас Григорович 2016 Ранок
Автори:Григорович О.В.
Видавництво:Ранок, Харьков
Рік видання:2016
Язык обучения:Украинский (ответы)
Відповіді до:Підручника (решебник)
СХОЖІ ГДЗ І ПІДРУЧНИКИ
Ответы Зошит практичних Хімія 8 клас Григорович. ГДЗ
підручник
Ответы к учебнику Химия 8 класс Григорович — решебник 2016
Повторення найважливіших питань курсу хімії 7 класу№ § 1. — § 3.
§ 1. Найважливіші хімічні поняття№ Стр. 5 — 10
§ 2. Кисень та вода. Реакції розкладу, сполучення№ Стр. 11 — 12
§ 3. Обчислення за формулами хімічних речовин№ Стр. 13 — 16
ТЕМА 1. Періодичний закон і Періодична система№ § 4. — § 16.
§ 4. Перші спроби класифікації хімічних елементів№ Стр. 17 — 22
§ 5. Поняття про лужні елементи,№ Стр. 23 — 26
§ 6. Періодичний закон Д. І. Менделєєва№ Стр. 27 — 31
І. Менделєєва№ Стр. 27 — 31
§ 7. Періодична система хімічних елементів.
§ 8. Значення Періодичного закону.
§ 9. Атом: ядро плюс електрони.
§ 10. Нукліди. Ізотопи
§ 11. Рух електронів у атомі. Електронні орбіталі
§ 12. Структура електронної оболонки атома
§ 13. Розподіл електронів в електронній оболонці атомів
§ 14. Будова електронних оболонок атомів
§ 15. Будова електронних оболонок хімічних елементів
§ 16. Характеристика хімічних елементів
ТЕМА 2. Хімічний зв’язок і будова речовини
§ 17. Природа хімічного зв’язку
§ 18. Ковалентний зв’язок
§ 19. Полярний і неполярний ковалентний зв’язок
§ 20. Йонний зв’язок
§ 21. Ступінь окиснення елементів
§ 22. Застосування поняття про ступінь окиснення
§ 23. Будова твердих речовин та їхні властивості
Лабораторний дослід № 1 — Домашній експеримент № 1.
ТЕМА 3. Кількість речовини. Розрахунки за хімічними формулами№ § 24. — § 27.
§ 24. Кількість речовини. Моль
Кількість речовини. Моль
§ 25. Молярна маса
§ 26. Молярний об’єм
§ 27. Відносна густина газів
ТЕМА 4. Основні класи неорганічних сполук№ § 28. — § 43.
§ 28. Класи неорганічних сполук
§ 29. Оксиди: фізичні властивості, поширеність
§ 30. Хімічні властивості оксидів
§ 31. Розрахунки за рівняннями хімічних реакцій
§ 32. Основи: фізичні властивості, поширеність
§ 33. Хімічні властивості лугів
Лабораторний дослід № 2 — Лабораторний дослід № 3№ Стр. 177 — 180
§ 34. Кислоти: фізичні властивості
§ 35. Хімічні властивості кислот
Лабораторний дослід № 4 — Домашній експеримент № 2
§ 36. Ряд активності металів.
Лабораторний дослід № 5 — Лабораторний дослід № 6 № Стр. 199 — 201
§ 37. Солі: фізичні властивості
§ 38. Хімічні властивості солей
Лабораторний дослід № 7 — Лабораторний дослід № 8
§ 39. Амфотерні оксиди й гідроксиди
§ 40. Способи добування оксидів
§ 41. Загальні способи добування кислот, основ та солей
§ 42.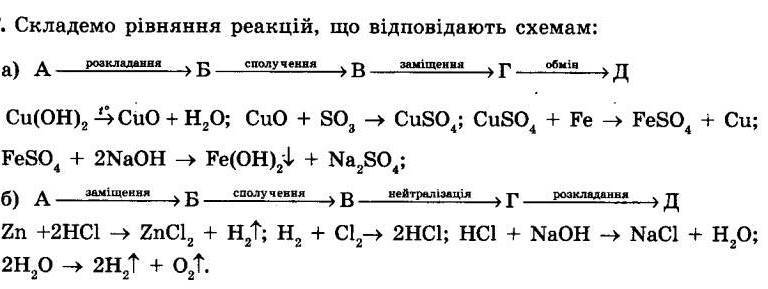 Генетичні зв’язки між класами неорганічних сполук
Генетичні зв’язки між класами неорганічних сполук
§ 43. Розв’язування експериментальних задач
ЛАБОРАТОРНІ ДОСЛІДИ та ПРАКТИЧНИ РОБОТИ№ 1 — 9
Лабораторний дослід №1
Лабораторний дослід №2
Лабораторний дослід №3
Лабораторний дослід №4
Лабораторний дослід №5
Лабораторний дослід №6
Лабораторний дослід №7
Лабораторний дослід №8
Лабораторний дослід №9
ПРАКТИЧНА РОБОТА № 1
ПРАКТИЧНА РОБОТА № 2
Поділитися:
Якщо є питання чи побажання пишіть у коментарі:
Учебник по Химии. 8 класс. Григорович
Учебник по Химии. 8 класс. Григорович — Новая программа
Этот учебник можно скачать в PDF формате на сайте тут.
Прочитати опис
Этот учебник — ваш главный помощник в изучении химии. Каждый параграф разделен на части. Небольшими порциями легче воспринимать информацию. Заканчивается параграф выводами и практическим блоком, состоящим из контрольных вопросов, заданий для усвоения материала. Некоторые вопросы обозначены звездочкой (*). Это задания проблемно-поискового содержания. На них вы не найдете ответа в тексте параграфа. Обратитесь к дополнительным источникам информации или обсудите эти вопросы на уроке.
Некоторые вопросы обозначены звездочкой (*). Это задания проблемно-поискового содержания. На них вы не найдете ответа в тексте параграфа. Обратитесь к дополнительным источникам информации или обсудите эти вопросы на уроке.
Повторение основных вопросов курса химии 7 класса
§ 1. Основные химические понятия
§ 2. Кислород и вода. Реакции разложения, соединения
§ 3. Вычисления по формулам химических веществ
Тема 1. Периодический закон и периодическая система химических элементов. Строение атома
§ 4. Первые попытки классификации химических элементов
§ 5. Щелочные элементы, галогены и инертные элементы
§ 6. Периодический закон Д. И. Менделеева
§ 7. Периодическая система химических элементов
§ 8. Значение Периодического закона. Научная прозорливость Д. И. Менделеева
§ 9. Атом: ядро плюс электроны
§ 10. Нуклиды. Изотопы
§ 11. Движение электронов в атоме. Электронные орбитали
§ 12. Структура электронной оболочки атома
§ 13. Распределение электронов в электронной оболочке атомов
Распределение электронов в электронной оболочке атомов
§ 14. Строение электронных оболочек атомов и структура Периодической системы
§ 15. Строение электронных оболочек и характер химических элементов
§ 16. Характеристика химических элементов по их месту в Периодической системе и строению атома
Тема 2. Химическая связь и строение вещества
§ 17. Природа химической связи
§ 18. Ковалентная связь
§ 19. Полярная и неполярная ковалентная связь
§ 20. Ионная связь
§ 21. Степень окисления элементов
§ 22. Применение понятия о степени окисления
§ 23. Строение твердых веществ и их свойства
Лабораторный опыт № 1. Ознакомление с физическими свойствами веществ атомного, молекулярного и ионного строения
Домашний эксперимент № 1. Изучение физических свойств веществ с разными типами кристаллических решеток: воды, поваренной соли, песка
Тема 3. Количество вещества. Расчеты по химическим формулам
§ 24. Количество вещества. Моль — единица количества вещества. Число Авогадро
Моль — единица количества вещества. Число Авогадро
§ 25. Молярная масса
§ 26. Молярный объем
§ 27. Относительная плотность газов
Тема 4. Основные классы неорганических соединений
§ 28. Классы неорганических соединений
§ 29. Оксиды: физические свойства, распространенность и применение
§ 30. Химические свойства оксидов
§ 31. Расчеты по уравнениям химических реакций
§ 32. Основания: физические свойства, распространенность и применение
§ 33. Химические свойства щелочей и нерастворимых гидроксидов
Лабораторный опыт № 2. Действие водных растворов щелочей на индикаторы
Лабораторный опыт № 3. Взаимодействие щелочей с кислотами в растворе
§ 34. Кислоты: физические свойства, распространенность и применение
§ 35. Химические свойства кислот
Лабораторный опыт № 4. Действие водных растворов кислот на индикаторы
Домашний эксперимент № 2. Действие на сок свеклы лимонного сока, раствора пищевой соды, мыльного раствора
§ 36. Ряд активности металлов. Реакции замещения
Ряд активности металлов. Реакции замещения
Лабораторный опыт № 5. Взаимодействие хлоридной кислоты с металлами
Лабораторный опыт № 6. Взаимодействие металлов с солями в водном растворе
§ 37. Соли: физические свойства, распространенностьи применение
§ 38. Химические свойства солей
Лабораторный опыт № 7. Взаимодействие солей со щелочами в водном растворе
Лабораторный опыт № 8. Реакция обмена между солями в растворе
§ 39. Амфотерные оксиды и гидроксиды
§ 40. Способы получения оксидов
§ 41. Общие способы получения кислот, оснований и солей
Практическая работа № 1. Изучение свойств основных классов неорганических соединений
§ 42. Генетические связи между классами неорганических соединений
§ 43. Решение экспериментальных задач
Лабораторный опыт № 9. Решение экспериментальных задач
Практическая работа № 2. Решение экспериментальных задач
Приложение 1. Распространенные соли и гидроксиды и их свойства
Приложение 2.
