Ответы к кроссворду «Химия 8 класс»
1: Наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения.
Ответ: химия
2: Таковой является смесь, в любой точке которой состав одинаков.
Ответ: гомогенная
3: Таковой является смесь, состав которой неодинаков в разных точках объёма.
Ответ: гетерогенная
4: Таковым является вещество, обладающее постоянными физическими свойствами.
Ответ: чистое
5: Способ разделения гетерогенной смеси с использованием жидкости.
Ответ: отстаивание
6: Процесс разделения гетерогенной смеси при помощи пористых материалов, задерживающих твёрдую фазу.
Ответ: фильтрование
7: Процесс получения чистого вещества из жидкости путём выпаривания.
Ответ: кристаллизация
8: Приём разделения гомогенных смесей путём испарения летучих жидкостей с последующей конденсацией их паров.
Ответ: дистилляция
9: Способ разделения смесей, основанный на различном поглощении разделяемых веществ поверхностью другого вещества.
Ответ: хроматография
10: Мельчайшая частица вещества, состоящая из атомов.
Ответ: молекула
11:
Мельчайшая химически неделимая частица вещества.Ответ: атом
12: Сложное вещество, образованное атомами разного вида.
Ответ: соединение
13: Вещество, образованное атомами одного вида.
Ответ: простое
14: Определённый вид атомов.
Ответ: элемент
15: Он у химически чистого вещества постоянен, независимо от места нахождения и способа получения.
Ответ: состав
16: Условная запись состава вещества посредством химических знаков и индексов.
17: Число, стоящее перед химической формулой.
Ответ: коэффициент
18: Число, которое записывается внизу справа от символа химического элемента.
Ответ: индекс
19: Свойство атома химического элемента присоединять или замещать определенное число атомов другого химического элемента.
Ответ: валентность
20: Условная запись химической реакции.
Ответ: уравнение
21: Химическая реакция, при которой из одного сложного получается два или несколько простых или сложных веществ.
22: Химическая реакция, при которой из двух или нескольких простых или сложных веществ образуется одно сложное вещество.
Ответ: соединения
23: Химическая реакция между простым и сложным веществом, при которой атомы простого вещества замещают атомы одного из элементов сложного вещества.
Ответ: замещения
24: Количество вещества, содержащее столько же частиц, сколько содержится атомов углерода в 0,012 кг углерода 12C.
Ответ: моль
25: Такая масса вещества — это масса одного моля вещества.
Ответ: молярная
26: Самый распространённый химический элемент в земной коре.
Ответ: кислород
27: Вещество, ускоряющее химическую реакцию, но в ней не участвующее.
Ответ: катализатор
28: Реакция окисления, при которой выделяется теплота и свет.
Ответ: горение
29: Сложное вещество из двух элементов, один из которых — кислород.
Ответ: оксид
30: Реакция, протекающая с выделением теплоты.
ВПР по химии 8 класс 2021 Варианты с ответами
В период с 15 марта по 21 мая 2021 года в очередной раз состоялись всероссийские проверочные работы по химии в 8 классах.
После проведения ВПР в школах стали доступны реальные варианты и критерии оценки.
Для каждой школы варианты формировались индивидуально из банка заданий ВПР.
→ купить рабочие тетради ВПР по химии для 8 класса
ВПР 2021 по химии для 8 класса с ответами
Структура проверочной работы ВПР 2021 по химии 8 класс
Вариант проверочной работы состоит из 9 заданий, которые различаются по содержанию и проверяемым требованиям.
Задания 1, 2, 7.3 основаны на изображениях конкретных объектов и процессов, требуют анализа этих изображений и применения химических знаний при решении практических задач.
Задание 5 построено на основе справочной информации и предполагает анализ реальной жизненной ситуации.
Задания 1, 3.1, 4, 6.2, 6.3, 8 и 9 требуют краткого ответа.
Остальные задания проверочной работы предполагают развернутый ответ.
КИМ ВПР 8 класса направлены на проверку у обучающихся предметных требований:
1) формирование первоначальных систематизированных представлений о веществах, их превращениях и практическом применении; овладение понятийным аппаратом и символическим языком химии;
2) осознание объективной значимости основ химической науки как области современного естествознания, химических превращений неорганических и органических веществ как основы многих явлений живой и неживой природы; углубление представлений о материальном единстве мира;
3) овладение основами химической грамотности: способностью анализировать и объективно оценивать жизненные ситуации, связанные с химией, навыками безопасного обращения с веществами, используемыми в повседневной жизни; умением анализировать и планировать экологически безопасное поведение в целях сохранения здоровья и окружающей среды;
4) формирование умений устанавливать связи между реально наблюдаемыми химическими явлениями и процессами, происходящими в микромире, объяснять причины многообразия веществ, зависимость их свойств от состава и строения, а также зависимость применения веществ от их свойств;
5) приобретение опыта использования различных методов изучения веществ: наблюдения за их превращениями при проведении несложных химических экспериментов с использованием лабораторного оборудования и приборов;
6) формирование представлений о значении химической науки в решении современных экологических проблем, в том числе в предотвращении техногенных и экологических катастроф.
Тексты заданий в КИМ ВПР 8 класса в целом соответствуют формулировкам, принятым в учебниках, включенных в Федеральный перечень учебников, допущенных к использованию при реализации имеющих государственную аккредитацию образовательных программ основного общего образования
Связанные страницы:
Демоверсия ВПР 2021 по химии 8 класс
Подготовка к ВПР по химии в 8 классе
Подготовка к ВПР по химии в 11 классе
Демоверсия ВПР 2021 по биологии 8 класс
Allied Solutions — Упрощенная химия для средней школы — Решения для 8-го класса по главе 5 «Язык химии»
Перейти к
- Иметь значение
- Физические и химические изменения
- Элементы, соединения и смеси
- Язык химии
- Химические реакции
- Водород
- Вода
- Углерод и его соединения
Главная > Решения Allied Solutions Химия класса 8 >
Упражнения в главе 5 язык химии 8 класс
Упражнение
Вопросы объективного типа
Вопросы в упражнении
Q1) Объясните термин «символ». Укажите причину, по которой символ кальция — «Ca», а меди — «Cu»
Укажите причину, по которой символ кальция — «Ca», а меди — «Cu»
Q2) Дайте определение термину «валентность». Относительно воды и аммиака как соединений укажите соответственно валентность кислорода и азота. Магний [[2, 8, 2]] имеет валентность 2+. Назови причины.
Q3) Объясните термин «переменная валентность». Медь с электронной конфигурацией [[2,8,18,1]] проявляет переменную валентность. Объясните причину и назовите соединение CuCl & CuCl_2
Q4) Укажите валентность следующих металлических элементов —
(а) Калий
(б) Натрий
(в) Кальций
(г) Магний
(д) Цинк
(е) Алюминий
(г) Хром
Q4) Некоторые металлы обладают переменной валентностью, включая валентность: 1+, 2+, 3+ и 4+. Укажите переменную валентность следующих металлов —
Укажите переменную валентность следующих металлов —
(а) Медь
(б) Серебро
(с) Меркурий
(г) Железо
(д) Олово
(f) Свинец
(а) Хлорид
(б) Бромид
(в) Йодид
(г) Нитрат
(д) Гидроксид
(е) Бикарбонат
(г) Бисульфит
(з) Бисульфат
(i) Алюминат
(к) Перманганат
(л) Оксид
(л) Сульфид
(м) Сульфит
(н) Сульфат
(о) Карбонат
(р) Дихромат
(к) цинкат
(р) Плюмбит
(с) Фосфат
(т) Нитрид
Q7) Различайте термины «ион» и «радикал» с подходящими примерами.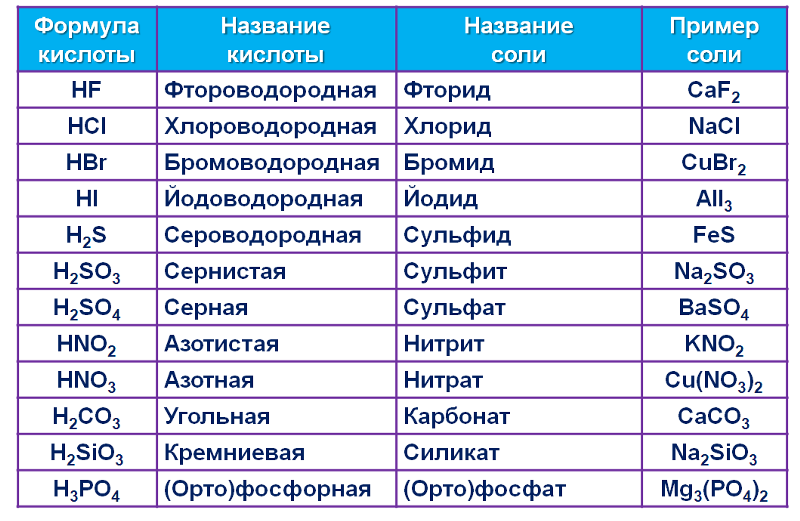
Q8) Напишите поэтапно химические формулы следующих соединений —
(а) Калий хлорид
(б) Бромид натрия
(с) Нитрат калия
(г) Гидроксид кальция
(e) Бикарбонат кальция
(е) Бисульфат натрия
(г) Сульфат калия
(h) Гидроксид цинка
(i) Перманганат калия
(к) Дихромат калия
(л) Гидроксид алюминия
(м) Нитрид магния
(м) Цинкат натрия
(n) Оксид меди [[II]]
(o) Медь [[I]] сульфид
(p) Железа [[III]] хлорид
(q) Гидроксид железа [[II]]
(r) Сульфид железа [[III]]
(s) Оксид железа [[III]]
Q9) Что такое химическое уравнение? Как это представлено. Проведите различие между «словным уравнением» и «молекулярным уравнением» на подходящем примере.
Q10) Укажите информацию, представленную химическим уравнением. Химические уравнения имеют ряд ограничений. Назовите основные ограничения химического уравнения.
Q11) Укажите, что такое сбалансированное уравнение, на соответствующем примере. Объясните, почему уравнение сбалансировано относительно закона сохранения материи.
Q12) Напишите сбалансированные молекулярные уравнения для слов уравнения:
Кальций + кислород → оксид кальция
Кальций + вода → гидроксид кальция + водород
Цинк + серная кислота → сульфат цинка + водород
Сульфат свинца + Гидроксид аммония → Сульфат аммония + Гидроксид свинца
Гидроксид меди + Азотная кислота → Нитрат меди + Вода
Нитрат свинца + хлорид натрия → Нитрат натрия + хлорид свинца
Вопросы объективного типа Вопросы
Q1) Дополните приведенные ниже утверждения, заполнив пропуск правильными словами.
- Формула хлорида серебра I: _____ [AgCl/AgCl_2]
- Основной единицей элемента является a/an _____ [[молекула/атом/ион]]
- Атом содержит _____ [[нетрон/ядро]] с положительно заряженными ________ [[электронами/протонами]]
- Элемент _______ [[кальций/свинец/углерод]] имеет символ, полученный из латинского слова «свинец».
- Из элементов — He, Br, Pt и O; элемент, который образует многоатомную молекулу, называется _____, а который является жидким при комнатной температуре, это ____.
- Валентность железа в FeO _____ [[2+/1+]], хлора [[хлорид]] в CaCl_2 ________ [[1-/2-]] и бихромата в K_2Cr_2O_7 ______ [[2+/ 2-]]
Q2) Сопоставьте утверждения — от 1 до 10 ниже с их правильными ответами от — A до J
| 1. Элементы, имеющие валентность два. | [[> виджет <]] |
2. Анион Анион | B: Двухвалентный |
| 3. Газообразный неметалл | C: Реагенты |
| 4. Катион А | D: Аммоний |
| 5. Термин, используемый для веществ, которые принимают участие в химической реакции | E: Оксид азота |
| 6. Значение символа ‘[[> виджет <]]' над стрелкой в химическом уравнении. | F: Азот |
| 7. Химическое название монооксида азота. | Г: Ноль |
| 8. Радикал, содержащий только азот и водород | H: Закись азота |
| 9. Химическое название закиси азота | I: требуется тепло |
| 10. Валентность благородных газов | J: [[> виджет <]] |
Q3) Сопоставьте соединения в списке I — от 1 до 20 с их правильными формулами в списке II — от A до T
1. Медь I Сульфид Медь I Сульфид | 2. Перманганат калия |
| 3. Фосфорная кислота | 4. Оксид меди I |
| 5. Углекислота | 6. Сульфид алюминия |
| 7. Оксид железа II | 8. Сульфид железа III |
| 9. Сульфат железа II | 10. Цинкат натрия |
| 11. Закись азота | 12. Сульфат алюминия |
| 13. Нитрид магния | 14. Сульфат железа III |
| 15. Оксид меди II | 16. Оксид железа III |
| 17. Оксид азота | 18. Сульфид меди II |
| 19. Сульфид железа II | 20. Нитрат магния |
А. [[> виджет <]] [[> виджет <]] | Б. [[> виджет <]] |
| C. [[> виджет <]] | Д. [[> виджет <]] |
| E. [[> виджет <]] | Ф. [[> виджет <]] |
| Г. [[> виджет <]] | Ч. [[> виджет <]] |
| I. [[> виджет <]] | Дж. [[> виджет <]] |
| К. [[> виджет <]] | Л. [[> виджет <]] |
| М. [[> виджет <]] | Н. [[> виджет <]] |
| О. [[> виджет <]] | стр. [[> виджет <]] |
| В. [[> виджет <]] | Р. [[> виджет <]] |
| С. [[> виджет <]] | Т. [[> виджет <]] |
Q4) Подчеркните неверно сбалансированное соединение в каждом уравнении и перепишите правильное уравнение:
- 2Na+3H_2O\ →\ 2NaOH+H_2
- 4P+4O_{2\ \ }→\ 2P_2O_5
- Fe_2O_3+2H_2\ →\ 2Fe\ +\ 3H_2O
- 2Al+2H_2SO_4\ →\ Al_2(SO_4)_3+3H_2
- N_2+3H_2\ →\ NH_3
- ZnO+3NaOH\ →\ Na_2ZnO_2+H_2O
- FeCl_3+3NH_4OH\ →\ 2NH_4Cl+Fe(OH)_3
- FeS+2HCl\ →\ 2FeCl_2+H_2S
- 3NH_3+H_2SO_4\ →\ (NH_4)_2SO_4
- PbO_2+4HCl\ →\ PbCl_2+H_2O+Cl_2
Фейсбук WhatsApp
Копировать ссылку
Было ли это полезно?
Главы в этой книге
Иметь значение
Физические и химические изменения
Элементы, соединения и смеси
Атомная структура
Язык химии
Химические реакции
Водород
Вода
Углерод и его соединения
Lido
Курсы
Быстрые ссылки
Условия и политика
Условия и политика
2022 © Quality Tutorials Pvt Ltd Все права защищены
Классы 6, 7 и 8 | Наука | Средняя школа | Химия
Элементарный (1–2 классы) Начальный (3–5 классы) Средний (6–8 классы) Младший средний (9–10 классы) Старший средний (11–12 классы) Испанский (все возрастные группы) ESL (все возрастные группы) GamesCup of Tea (для всех возрастов)
- Домашний
- Средняя школа: 6, 7 и 8 классы
- Наука: Средняя школа: 6, 7 и 8 классы
- Химия — атом
Химия в основном связана с атомами .
Эта викторина по естествознанию называется «Химия. Атом» и была написана учителями, чтобы помочь вам, если вы изучаете предмет в средней школе. Играя в образовательные викторины, вы учитесь в 6-м, 7-м или 8-м классе в возрасте от 11 до 14 лет. школьная работа. Вы можете подписаться на странице Присоединяйтесь к нам
Химия — это наука о составе, строении, свойствах и изменении вещества. В основном это касается атомов и их взаимодействий с другими атомами.
Атом — основная единица всей материи. Он содержит плотное центральное ядро, окруженное облаком отрицательно заряженных электронов. Оно происходит от греческого слова атомос , что буквально означает нечто неразделимое или неразделимое.
В центре атома или его ядре находится ядро . Ядро содержит протоны и нейтроны.
протон — это частица, несущая положительный электрический заряд.
Электрон — это частица, несущая отрицательный электрический заряд. Электроны определяют химические свойства элемента.
Электроны определяют химические свойства элемента.
Нейтрон — субатомная адронная частица, не имеющая электрического заряда. Его масса немного больше, чем у протона. Ядро каждого атома содержит по крайней мере один нейтрон, за исключением водорода-1. Нейтроны связываются с протонами, чтобы стабилизировать ядро атома.
Вместе протоны и нейтроны обозначаются как « нуклонов ”.
Количество протонов в ядре атома известно как атомный номер . Поскольку каждый элемент имеет разное количество протонов, у каждого элемента есть свой атомный номер.
Атом классифицируется по количеству нейтронов и протонов в его ядре. Количество протонов определяет химический элемент, а количество нейтронов определяет изотоп элемента.
Изотоп представляет собой вариант, содержащийся в определенном химическом элементе. Изотопы имеют одинаковое количество протонов в каждом атоме, но количество нейтронов может варьироваться.
Элемент — это любое вещество, которое нельзя разбить на два или более простых вещества. Есть четыре общих элемента, которые включают землю, воздух, воду и огонь.
Есть четыре общих элемента, которые включают землю, воздух, воду и огонь.
Химический элемент представляет собой вещество, состоящее из атомов одного типа. Химические элементы делятся на металлы, металлоиды и неметаллы. Примеры включают углерод, азот, кислород, кремний, алюминий, железо, золото, свинец, ртуть, медь и мышьяк. К самым легким химическим элементам относятся гелий, водород, литий и бериллий. Любые два атома, имеющие одинаковое количество протонов в соответствующих ядрах, принадлежат к одному и тому же химическому элементу.
1.
Любое вещество, которое нельзя разделить на два или более простых вещества, называется _______.
элемент
субатомная частица адрона
химический элемент
изотоп
2.
Центр или ядро атома называется ______.
атом
нейтрон
ядро
нуклон
3.
Он содержит плотное центральное ядро, окруженное облаком отрицательно заряженных электронов.
Протон
Электрон
Нейтрон
Атом
4.
Греческое слово атомос означает ______.
атомный номер
количество нейтронов
отрицательные и положительные заряды
неразделимое или то, что нельзя разделить
5.
Изучение состава, структуры, свойств и изменений материи известно как _______.
материя
атомы
физика
химия
6.
Число протонов в ядре атома известно как ________.
субатомная частица адрона
атомный номер
нуклон
нейтрон фактор
7.
Это частица, несущая положительный электрический заряд.
Нейтрон
Ион
Протон
Электрон
8.
Вещество, состоящее из атомов одного типа, _________.
химический элемент
элемент
ядра
изотоп
9.
Это частица, несущая отрицательный электрический заряд.
Ион
Электрон
Протон
Нейтрон
10.
